17 kwietnia 2025
Życzenia świąteczne
Szanowni Państwo, z okazji zbliżających się Świąt Wielkanocnych życzymy, by ten wyjątkowy czas przyniósł wytchnienie w codziennych troskach oraz wiele radości i nadziei. Redakcja Portalu Hemopozytywni.pl


17 kwietnia 2025
Szanowni Państwo, z okazji zbliżających się Świąt Wielkanocnych życzymy, by ten wyjątkowy czas przyniósł wytchnienie w codziennych troskach oraz wiele radości i nadziei. Redakcja Portalu Hemopozytywni.pl

Około 50% polskiego społeczeństwa choruje na choroby przewlekłe, w tym, według danych statystycznych, nawet 46 000 osób na hemofilię. 17 kwietnia na całym świecie obchodzony jest Dzień Świadomości Hemofilii. Jest to okazja do informowania i edukowania o tej złożonej chorobie występującej w trzech postaciach: łagodnej, umiarkowanej i ostrej. W zależności od postaci, hemofilia jest diagnozowana na różnych etapach życia i wymaga zróżnicowanych ścieżek leczenia. W postaci ostrej czynnik krzepnięcia krwi podawany jest nawet co 48 godzin, w łagodniejszych formach, tylko zapobiegawczo, gdy dochodzi do wypadków i urazów. Życie z chorobą przewlekłą, która nieleczona uszkadza organizm, odbiera zdrowie, a w najgorszych przypadkach nawet życie jest wymagające i stresujące, w szczególności, gdy chorują dzieci. Światowe obchody dni chorób to bardzo ważna inicjatywa mająca na celu edukowanie i zwracanie uwagi społeczeństwa na problemy, z którymi na co dzień, na całym świecie zmaga się coraz większa liczba osób. Niestety statystyki pokazują, że liczba osób chorych przewlekle i chorych na choroby rzadkie rośnie każdego roku. Codziennie mijamy osoby, które wyglądają na w pełni zdrowe, a chorują na choroby o których prawdopodobnie nigdy nie słyszeliśmy i nie zdajemy sobie sprawy, w jak dużym stopniu wpływają one na ich codzienność oraz ich najbliższych. Hemofilia należy do tzw. chorób niewidzialnych – takich, których objawy nie są dostrzegalne na pierwszy rzut oka. Osoba żyjąca z hemofilią nie zdradza zewnętrznych oznak choroby, ponieważ jej istotą jest niewidoczny deficyt czynnika krzepnięcia krwi. Niestety, to właśnie niewidoczność objawów stanowi jedno z największych zagrożeń dla osób chorych, zwłaszcza w sytuacjach nagłych, takich jak wypadki komunikacyjne czy utrata przytomności. Bardzo istotne jest, aby całe społeczeństwo było edukowane na temat znaczenia noszenia przy sobie informacji o chorobie w przypadku schorzeń przewlekłych. Przykładem może być opaska z napisem „Mam hemofilię”, która w sytuacji zagrożenia życia pozwala osobie udzielającej pomocy szybko poinformować o tym służby ratunkowe. Dlatego właśnie tak ważne są kampanie zwiększające świadomość na temat rzadkich i mniej znanych chorób. W tym roku poprosiliśmy o wypowiedź dwie kobiety, które na hemofilii znają się bardzo dobrze. Jedną z nich jest Pani Ania, mama 9-letniego Frania chorującego na hemofilię, a drugą - dr Irena Woźnica-Karczmarz, pediatra, onkolog i hematolog dziecięcy, a także transfuzjolog kliniczny z Uniwersyteckiego Szpitala Dziecięcego w Lublinie. Czym jest hemofilia? Hemofilia jest wrodzoną i w większości przypadków, uwarunkowaną genetycznie skazą krwotoczną, polegającą na niedoborze lub całkowitym braku jednego z czynników krzepnięcia. Matka nosicielka może przekazać wadliwy gen, który zlokalizowany jest na chromosomie X. Ryzyko, że dziecko go odziedziczy wynosi 50% Jeśli syn odziedziczy zmutowany gen, na pewno zachoruje, jeśli dostanie go córka, to będzie nosicielką, ale nie zachoruje. Żeby tak się stało, musiałaby dostać wadliwy gen i na chromosomie X od matki, i na chromosomie X od ojca lub nie mieć prawidłowego chromosomu X, co może mieć miejsce np. w zespole Turnera. Takie sytuacje zdarzają się niezwykle rzadko. Gdy na hemofilię choruje ojciec, a matka nie jest nosicielką i jest zdrowa, wszystkie jego córki będą nosicielkami, a synowie będą zdrowi. Nowe mutacje genetyczne są odpowiedzialne za około 30% zachorowań w rodzinach, w których nikt nie cierpiał na tę chorobę, a matka nie jest jej nosicielką. Oznaki ostrzegawcze Typowe oznaki hemofilii, na które rodzice powinni reagować i od razu zgłaszać się do lekarza pediatry to: znaczne wylewy po pierwszych szczepieniach, zastrzykach, duże siniaki po pobraniach krwi, skłonność do dużych, guzowatych siniaków, krwawienia do pośladka lub do uda, dłuższe krwawienia dziąseł związane z ząbkowaniem, duże – znacznie większe niż u rówieśników – wylewy, np. na łokciach czy pupie powstające podczas raczkowania i związane z pierwszymi upadkami, utykanie małego dziecka na jedną nóżkę, u dziewczynek w okresie dojrzewania przedłużające się i bardzo obfite miesiączki. Pediatra po ocenie objawów i zleceniu badań, powinien kierować dziecko z podejrzeniem skazy krwotocznej do specjalisty, czyli lekarza hematologa. „Z perspektywy lekarza bardzo istotne jest, by uważnie słuchać i wyłapywać wszelkie informacje przekazywane przez rodziców podczas wizyty. To oni najlepiej znają swoje dziecko, potrafią zauważyć zmiany w zachowaniu i niuanse w wyglądzie, które mogą sugerować wystąpienie choroby. Nie możemy bagatelizować obaw rodziców, ich intuicja jest bezcenna” – dodaje dr Woźnica-Karczmarz. Czynniki krzepnięcia W przypadku hemofilii A w organizmie występuje deficyt czynnika VIII, w hemofilii B czynnika IX, a w hemofilii typu C, czynnika XI. W zależności od stopnia niedoboru czynnika krzepnięcia krwi wyróżnia się trzy postacie hemofilii: ciężką, gdy poziom czynnika w krwi nie przekracza 1%, umiarkowaną, gdy osiąga od 1 do 5% oraz łagodną, gdy czynnik krzepnięcia wynosi od 5 do 50%. Każdy z typów hemofilii może mieć postać łagodną, umiarkowaną lub ostrą. U osób zdrowych, czynnik krzepnięcia utrzymuje się stale na poziomie pomiędzy 50 a 150%. Oznacza to, że w przypadku urazu lub zabiegu, gdy dochodzi do naruszenia naczyń krwionośnych, dzięki czynnikowi krzepnięcia, krew osoby zdrowiej krzepnie samoczynnie nie dopuszczając do krwotoku. W przypadku osób chorych, u których czynnik nie występuje lub występuje w zbyt małej ilości, krwawienia są trudne lub niemożliwe do zatrzymania, tworzą się nieadekwatnie duże, guzowate siniaki, które wchłaniają się bardzo powoli i niezbędne jest zastosowanie specjalnych maści, aby przyspieszyć proces gojenia. Krwawienia samoistne W Polsce najczęstszym typem hemofilii jest typ A i choruje na nią 1 na 12 300 mieszkańców. W postaci ciężkiej każdego typu hemofilii może dochodzić do samoistnego występowania krwawień, które uszkadzają organy wewnętrzne. Oznacza to, że nawet bez wystąpienia urazu, uderzenia, a nawet bez zwiększonej aktywności fizycznej może dojść do krwotoku wewnętrznego. Świadomość występowania choroby w rodzinie i mówienie o tym otwarcie jest kluczowe w procesie diagnostyki nowo narodzonych dzieci. Im szybciej pacjent zostanie zdiagnozowany, tym szybciej lekarze mogą wdrożyć leczenie profilaktyczne i zapobiec nieodwracalnym zmianom w organizmie. Najbardziej niebezpieczne są zagrażające życiu krwawienia do mózgu, stawów i narządów wewnętrznych. Częste i powtarzające się krwawienia do stawów powodują ich trwałe uszkodzenia. Nieleczeni pacjenci z ostrą postacią hemofilii cierpią na kontuzje wywołane krwawieniami, które doprowadzają ich do trwałego kalectwa, a w ekstremalnych przypadkach mogą nawet prowadzić do śmierci. 100 lat temu i przed wdrożeniem nowoczesnych form terapii, dzieci z hemofilią dożywały średnio 9-10 lat. Wiadomo, że było to związane z ciężkimi krwawieniami do centralnego układu nerwowego, do jamy brzusznej i oczywiście do stawów; w wyniku czego dzieci szybko stawały się niepełnosprawne. Jedyne co można było im zaoferować to łagodzenie bólu towarzyszącego krwawieniom, a ten przy wylewie do stawu jest naprawdę bardzo silny. Obecnie, dzieci z ciężką postacią hemofilii są skutecznie leczone i przy zachowaniu odpowiednich środków bezpieczeństwa, takich jak np. unikanie sportów kontaktowych generujących urazy lub korzystanie z aplikacji informującej o poziomie czynnika krzepnięcia w krwi, mogą prowadzić satysfakcjonujące życie. Historia rodzinna „Niestety nie wykonuje się badań przesiewowych w kierunku hemofilii. Jeżeli w rodzinie występuje hemofilia i mama poinformuje o tym fakcie lekarzy, to neonatolodzy mają obowiązek wykonania badań bezpośrednio po urodzeniu albo nawet z krwi pępowinowej” – informuje dr Woźnica – Karczmarz. „W naszym przypadku najbardziej stresująca była druga ciąża i moment, w którym dowiedzieliśmy się, że na świecie ma pojawić się drugi syn. Ryzyko, że tak jak starszy brat będzie nosicielem wadliwego genu wynosiło 50%. Pani doktor prowadząca moją ciążę zleciła pobranie próbki krwi z krwi pępowinowej, ale ostatecznie z nieznanego mi powodu to badanie się nie powiodło. Na wynik kolejnych badań czekaliśmy bardzo długo i to było bardzo stresujące. Wiedzieliśmy już wtedy na temat hemofilii bardzo dużo. Na szczęście drugi syn jest zdrowy. Nasz pierwszy syn Franek, choruje na łagodną postać hemofilii typu A. Dowiedzieliśmy się o tym, gdy miał około pół roku i zaczął się więcej ruszać. Nagle, bez wyraźnego urazu, na jego kolanie pojawił się siniak, który był bardzo duży i nie znikał samoczynnie przez dłuższy czas. To zwróciło naszą uwagę i było pretekstem do tego, by „połączyć kropki” medycznej historii rodzinnej. Dziadek Frania, mój tata, miał stwierdzoną łagodną postać hemofilii w dorosłym życiu, przy okazji prostego zabiegu usunięcia zęba, po którym pojawiło się nieznacznie większe niż zazwyczaj krwawienie. Zlecono wtedy badania pod kątem hemofilii i potwierdzono jej bardzo łagodną postać. Jako że nie wiązało się to z koniecznością przyjmowania leków i nie zmieniło codzienności taty, choroba nie wzbudziła naszych obaw. Na tamtym etapie nie dotarła do nas informacja, że łagodna postać hemofilii mojego taty, może mieć wpływ na życie jego wnuków. Wtedy jeszcze niewiele wiedzieliśmy o hemofilii i w naszej świadomości, nie było potrzeby, aby zgłębiać temat w kontekście naszych dzieci. Krwawienie taty samoistnie ustało, a temat hemofilii w naszej rodzinie ucichł. Franek urodził się jako zdrowy chłopiec i nic nie wskazywało na to, że będzie na coś chory. Ja nie zgłaszałam faktu występowania hemofilii w rodzinie lekarzom, ani w ciąży, ani po porodzie, bo nie miałam świadomości, że może to być ważna informacja i że choroba może mieć wpływ na moje dzieci. Bardziej skupiona byłam na tym, że w ciąży wystąpiła u mnie cholestaza i wszelkie obawy o dziecko wynikały tylko z niej” – opowiada Pani Ania, która jest nosicielką hemofilii. „W rodzinach, w których występuje hemofilia i została ona wcześniej zdiagnozowana oraz leczona, osoby chore zazwyczaj informują swoich bliskich o możliwości dziedziczenia choroby. Dzięki temu przyszli rodzice są bardziej świadomi jej specyfiki i mają czas, aby przygotować się psychicznie na ewentualne wystąpienie hemofilii u swoich dzieci. Zupełnie inaczej wygląda sytuacja w przypadku rodzin, w których wcześniej nie odnotowano przypadków tej choroby. Rodzice przychodzący na wizytę do hematologa często nie posiadają żadnej wiedzy na temat hemofilii, a sama diagnoza bywa dla nich druzgocąca – niesie ze sobą poważne zagrożenie dla życia małego dziecka i może prowadzić do silnych reakcji emocjonalnych rodziców, w tym nawet stanów depresyjnych. Dlatego tak istotne jest szybkie określenie typu hemofilii, uspokojenie rodziców oraz przedstawienie jasnego planu działania na najbliższe dni i miesiące. Taki plan daje poczucie bezpieczeństwa, a wsparcie udzielone przez lekarza prowadzącego jest w tej sytuacji nie do przecenienia” – podkreśla doktor Woźnica-Karczmarz. Rozpoznanie „Mamy ogromne szczęście, że nasz syn jest pod opieką wspaniałej pani doktor Woźnicy-Karczmarz. Jej zaangażowanie w proces leczenia, otwartość na nasze pytania – niezależnie od pory dnia – oraz empatia, jaką nas obdarza, dają nam ogromne poczucie bezpieczeństwa” – mówi mama 9-letniego Frania, który zmaga się z łagodną postacią hemofilii typu A. Edukowanie rodziny i otoczenia dziecka na temat hemofilii, nowoczesnych możliwości terapeutycznych oraz – co najważniejsze – przekazywanie nadziei, że z tą chorobą można prowadzić normalne życie, to ogromna odpowiedzialność spoczywająca na lekarzu prowadzącym. Kluczowe jest zwrócenie uwagi na detale, które decydują o codziennym funkcjonowaniu chorego – od wyzwań, przed którymi stają rodzice, po konkretne działania, takie jak zabezpieczenie mebli czy dostosowanie przestrzeni domowej, aby zapobiegać urazom. Dla zdrowego dziecka to drobnostki, ale dla dziecka z ciężką postacią hemofilii mogą one oznaczać realne zagrożenie w postaci trudnych do zatrzymania krwotoków wewnętrznych. „Poinformowanie rodziców, że ich dziecko cierpi na skazę krwotoczną, to jeden z najtrudniejszych momentów w całym procesie leczenia” – przyznaje dr Woźnica-Karczmarz. „Od tej pierwszej rozmowy często zależy stan psychiczny rodzica, jego podejście do choroby oraz gotowość do współpracy w dalszym leczeniu” – dodaje specjalista. W przypadku dzieci z ciężką postacią hemofilii diagnoza bywa szokiem. Dlatego tak ważne jest, aby lekarz potrafił nie tylko rzeczowo i przystępnie przekazać informacje medyczne, ale również uważnie wsłuchać się w potrzeby rodziny. „Aby realnie wesprzeć rodziców w tak trudnej chwili, warto od początku rozważyć także włączenie wsparcia psychologicznego, a niekiedy również psychiatrycznego” – zaznacza dr Woźnica-Karczmarz. Łagodna postać Każda choroba – niezależnie od tego, czy ma łagodny czy cięższy przebieg – stanowi ogromne obciążenie psychiczne nie tylko dla rodziców chorego dziecka, ale i dla całej rodziny. Zarówno stres, jak i sama hemofilia, często pozostają niewidoczne na pierwszy rzut oka. Gdy dziecko rośnie, nabiera pewności w poruszaniu się i nie upada już przy każdym kroku, codzienne życie staje się odrobinę łatwiejsze. Jednak napięcie związane z chorobą nie znika. W przypadku łagodnej postaci hemofilii, leczenie nie jest potrzebne na co dzień – o ile nie dojdzie do urazu, który mógłby stanowić realne zagrożenie. Mimo to rodzicielskie obawy i niepokój wciąż towarzyszą każdemu etapowi rozwoju dziecka. Pani Ania, mama 9-letniego Frania, dzieli się swoim doświadczeniem wychowywania dziecka z łagodną postacią hemofilii: „Nasz syn uczęszczał do przedszkola, a teraz jest już aktywnym, ciekawym świata uczniem drugiej klasy. Uwielbia sport i przez pewien czas uczęszczał na zajęcia karate. Nigdy nie doszło do żadnych poważniejszych urazów podczas treningów. Zrezygnował, bo zajęcia przestały go cieszyć. Staramy się nie być nadopiekuńczy ani nadmiernie przestraszeni, bo wiemy, że taka postawa nie sprzyja jego rozwojowi. Najwięcej stresu – zarówno dla nas, jak i dla Frania – wiąże się z podawaniem czynnika krzepnięcia dożylnie. To są trudne momenty. Największym wyzwaniem jest jednak pogodzenie naszej potrzeby, by Franek poznawał świat równie intensywnie jak jego rówieśnicy, z lękiem przed tym, co może się wydarzyć – jeśli się przewróci, spadnie z drabinek, czy zrani w czasie zabawy. Naturalne jest, że instynktownie jesteśmy bardziej ostrożni. Myślę, że nasza postawa, choć zrozumiała, mogła wpłynąć na większą ostrożność Frania w porównaniu z jego bratem”. Choroba chłopców Hemofilia jest chorobą genetyczną sprzężoną z płcią. W przeważającej większości chorują na nią mężczyźni, a kobiety stanowią bardzo mały procent wszystkich chorych. Nie oznacza to jednak, że powinny być pomijane w dyskursie o chorobie. Światowa Federacja ds. Hemofilii (WFH) z okazji obchodów dnia hemofilii, przypadającego 17 kwietnia, w 2025 roku zainaugurowała kampanię świadomości Women & Girls bleed too mówiącą o tym, że kobiety i dziewczynki chorują na hemofilię i także doświadczają problemów związanych z deficytem czynnika krzepnięcia, takich jak ból, konieczność przyjmowania czynnika oraz zachowywania ostrożności w codziennych aktywnościach. Dodatkowo hemofilia u kobiet może oznaczać wydłużone, bardziej obfite i dokuczliwe miesiączki. Wiadomo też, że kobiety często nie zdają sobie sprawy z tego, że będąc nosicielkami mogą mieć objawy łagodnej hemofilii. „Często podczas wywiadu z pacjentką pytam o krwawienia miesiączkowe. Kobiety z reguły mówią, że ich krwawienie jest normalne, jednak, gdy odpowiadają na dodatkowe, bardziej szczegółowe pytania okazuje się, że miesiączka trwa dwa tygodnie, a podpaski lub tampony są wymieniane co godzinę. To nie jest normalne, choć historia rodzinna podpowiada, że tak ma być, bo mama, siostra, babcia i ciocia w ten sposób miesiączkują. Takie kobiety nie wiedzą, że prawdopodobnie wszystkie w ich rodzinie są chore. Jestem przekonana, że zawodzi system, który nie edukuje w odpowiedni sposób. Gdy ja chodziłam do szkoły, uczono nas na lekcjach biologii między innymi o tym, jak wygląda prawidłowy okres” – stwierdza dr Woźnica-Karczmarz z Uniwersyteckiego Szpitala Dziecięcego w Lublinie. Przedszkole i szkoła „Ważne jest, żeby dzieci uczestniczyły we wszystkich zabawach z rówieśnikami, szczególnie w tym wieku, ponieważ aktywności fizyczne wśród małych dzieci nie sprawiają zwykle więcej problemów za wyjątkiem okazjonalnego siniaka. Przy zranieniach i zadrapaniach wystarczy zwykle standardowa pierwsza pomoc” – czytamy w przewodniku dla szkół opracowanym przez The Haemophilia Society, przetłumaczonym na język polski. „Zarówno w przedszkolu jak i w szkole spotkaliśmy się z pełnym zrozumieniem dyrekcji i personelu placówek. Na początku każdego etapu edukacji w placówkach naszym zadaniem było zapoznać nauczycieli ze specyfiką choroby. Na podstawie zaleceń lekarskich, opisanych w przystępnej formie broszury, a także własnych doświadczeń, mąż przygotował informacje o chorobie i o tym w jakich przypadkach należy zwrócić szczególną uwagę na naszego syna. Pani wychowawczyni w szkole zapewniła nas, że czuje się odpowiednio poinformowana i nie potrzebuje dodatkowych wyjaśnień z naszej strony. Często, chcąc „dmuchać na zimne”, informowała nas o nawet najmniejszych zajściach z udziałem Frania, takich jak np. to, że został popchnięty przez kolegów lub lekko się o coś uderzył. W takich sytuacjach uspokajaliśmy Panią, że w razie niepewności warto postępować tak jak w przypadku zdrowych dzieci, czyli jeśli doszło do urazu to należy przyłożyć coś zimnego w miejscu zranienia. Aby zapewnić najwyższą możliwą formę opieki nad naszym synem ustaliliśmy ze szkołą i wychowawczynią, że jedna dawka czynnika będzie przechowywana w szkole w razie wystąpienia cięższego urazu i konieczności wezwania karetki. To, że czynnik jest dostępny w szkole, zdecydowanie skraca czas podania go, bo medycy, którzy dotrą do szkoły mogą to zrobić na miejscu lub w karetce w drodze do szpitala. Niestety nie w każdym szpitalu odpowiedni czynnik krzepnięcia jest dostępny od ręki. Świadomość, że mamy zabezpieczoną dawkę czynnika w szkole daje nam bardzo duże poczucie bezpieczeństwa. Na szczęście w ciągu półtora roku obecności syna w szkole, nie było konieczności wykorzystania go. Nauczyciele nie są przeszkoleni z podawania czynnika krzepnięcia, jest to zbyt skomplikowane i wymaga umiejętności wkłucia się w żyłę” – opowiada mama Frania. Możliwe leczenie „Naszym nadrzędnym celem jest osiągnięcie u pacjenta takiego poziomu czynnika krzepnięcia krwi, który pozwala przekształcić ciężką postać hemofilii w umiarkowaną, a najlepiej – łagodną. Dążymy do tego, aby poziom czynnika utrzymywał się na stałe powyżej 5%, a optymalnie wynosił około 12%, ponieważ wtedy mamy pewność, że nie wystąpią samoistne krwawienia – szczególnie te najgroźniejsze, jak krwawienia do ośrodkowego układu nerwowego” – mówi dr Woźnica-Karczmarz. Leczenie jest indywidualnie dostosowywane do farmakokinetyki oraz stylu życia pacjenta, w tym poziomu jego aktywności fizycznej. Podawanie czynnika krzepnięcia odbywa się zazwyczaj co 48 godzin. Taka forma profilaktyki pozwala utrzymać aktywność czynnika krzepnięcia na poziomie kilku lub kilkunastu procent, co skutecznie chroni pacjenta przed groźnymi, samoistnymi krwawieniami charakterystycznymi dla ciężkich postaci hemofilii. Po rozpoznaniu choroby dziecka, kolejnym krokiem jest podjęcie decyzji o tym, jaką formę leczenia należy zastosować i kiedy ją rozpocząć. Dzieci z ciężką postacią hemofilii mają zagwarantowaną profilaktykę krwawień, czyli leczenie od urodzenia do ukończenia 18. roku życia czynnikami rekombinowanymi, bardzo bezpiecznymi i nie dającymi powikłań. Program rozpoczął się w 2008 roku i jest finansowany przez NFZ. W czerwcu 2024 roku do programu weszła zmiana, która umożliwia u najmłodszych dzieci do drugiego roku życia włączenie leków podawanych podskórnie. Wcześniej leczenie tak małych dzieci polegało na założeniu dostępu centralnego, co wiązało się z interwencją chirurgiczną. Stosowanie dostępów centralnych często powodowało powikłania takie jak zakażenia czy zakrzepice. Rodzice musieli podawać leki poprzez wkłucie centralne, co także nie jest łatwe i wymaga wiedzy, przeszkolenia, odwagi, precyzji i zachowania rygorystycznych zasad higieny. Nie wszyscy rodzice, jest to w pełni zrozumiałe, czuli się z taką formą podań komfortowo. Podawanie czynnika krzepnięcia podskórnie znacząco odmieniło życie najmłodszych dzieci z ciężką postacią hemofilii, a także ich dzielnych rodziców. Obecnie terapia genowa w hemofilii nie jest dostępna dla dzieci – została zarejestrowana wyłącznie dla pacjentów dorosłych i nic nie wskazuje na to, by w najbliższym czasie miało się to zmienić. Wszystkie dotychczasowe badania kliniczne prowadzone były wyłącznie wśród osób dorosłych. Co więcej, podczas stosowania terapii genowych mogą wystąpić działania niepożądane, takie jak uszkodzenie wątroby, dlatego lekarze nie mają ani odpowiednich danych, ani przekonania, by stosować tego typu leczenie u najmłodszych pacjentów. Terapia genowa może wprawdzie czasowo zwiększyć poziom czynnika krzepnięcia, jednak z biegiem czasu jego stężenie stopniowo maleje. W przypadku łagodnej postaci hemofilii czynnik krzepnięcia podaje się doraźnie – najczęściej po urazach. Kluczową rolę odgrywa tu rodzic, który we współpracy z lekarzem ocenia stopień urazu i dobiera odpowiednią dawkę czynnika, dostosowaną do masy ciała dziecka. Aplikacja – na czym ona polega? Żeby wiedzieć dokładnie, ile czynnika należy podać, opracowano aplikację, która informuje o tym, jaki jest aktualny poziom czynnika krzepnięcia. Aplikacja ma ikonę bateryjki. Musi zostać pobrana przez lekarza prowadzącego i indywidualnie skalibrowana dla każdego pacjenta, co oznacza, że do aplikacji trzeba wprowadzić dane, takie jak krzywa obniżania się czynnika krzepnięcia w krwi. Gdy ikona pokazuje kolor zielony - oznacza to wysoki poziom czynnika i pełne zabezpieczenie. Żółta wskazuje, że czynnika zaczyna brakować i należy zachować ostrożność, a czerwona, że poziom przekroczył próg bezpieczeństwa i łatwo może dojść do samoistnych krwawień. Następnie na bieżąco dodaje się informację, kiedy pacjent dostał czynnik. Dzięki tej aplikacji pacjenci dokładnie wiedzą, kiedy mogą biegać, skakać i szaleć, a kiedy już muszą otrzymać czynnik krzepnięcia. Wsparcie „Ogromnym wsparciem dla nas jest nasza pani doktor, która zawsze reaguje na nasze pytania w chwilach wątpliwości – czy podawać już czynnik, czy możemy się jeszcze wstrzymać, konsultuje przesłane zdjęcia i podpowiada, jak działać. Jest cierpliwa, otwarta i bardzo serdeczna. Pani doktor wystawiła dla nas zaświadczenie podróżne o przewożonym zestawie niezbędnym do podawania czynnika, który zawiera igły, poinstruowała o konieczności zakupu mini torby-lodówki, która zapewnia odpowiednią temperaturę ampułki z czynnikiem. Pani dr Woźnica-Karczmarz powiedziała nam o Stowarzyszeniu Osób Chorych na Hemofilię działającym w Lublinie, do którego należymy. Coroczne spotkania z rodzicami dzieci chorych na hemofilię są bardzo wspierające, dają poczucie, że nie jesteśmy całkiem sami z chorobą naszego syna. W naszym środowisku nie ma innych dzieci chorych na hemofilię, z którymi moglibyśmy ponarzekać, podzielić się troskami, ale także nową wiedzą i sukcesami dzieci. Spotkania mają formę praktycznych warsztatów, podczas których przekazywana jest spora dawka wiedzy, np. uczymy się odpowiedniego wkłuwania się w żyłę i podawania czynnika. Są ciekawe także dla naszego syna, który spotyka się z innymi dziećmi chorymi na hemofilię, które rozumieją, z czym on mierzy się na co dzień. Dzięki stowarzyszeniu i jego działaniom, hemofilia kojarzy się dzieciom także z corocznymi ciekawymi spotkaniami z fajnymi ludźmi, a nie tylko z bolesnym podawaniem czynnika. Dla nas to bardzo ważne, że syn widzi także korzyści, a nie wyłącznie koszty choroby" – podsumowuje Pani Ania. Na podstawie: hematoonkologia.pl haemophilia.org.uk onkologia-dziecieca.pl wfh.org wum.edu.pl

10 marca 2025
Serdecznie zapraszamy do obejrzenia II części debaty eksperckiej pt. „Personalizacja profilaktyki hemofilii A – skuteczność i bezpieczeństwo terapii”, podczas której eksperci omówili postępy w leczeniu hemofilii u dzieci, z uwzględnieniem włączenia pacjentów z ciężką postacią hemofilii A do profilaktyki. https://vimeo.com/1047855814/9014498c6e Dyskusja, poprowadzona przez prof. Pawła Łagunę, kierownika Kliniki Hematologii Dziecięcej i Transplantologii Klinicznej Warszawskiego Uniwersytetu Medycznego, w której udział wzięli prof. Anna Klukowska, prof. Tomasz Urasiński, dr Andrzej Kołtan, skupiła się wokół postępów w leczeniu hemofilii A u dzieci, ze szczególnym uwzględnieniem personalizacji profilaktyki. „To spersonalizowanie profilaktyki, czyli indywidualizacja, czyli dostosowanie do danego pacjenta, co związane jest również z jego wiekiem, z jego aktywnością, etapem życiowym tym, co chce robić: czy chce grać w piłkę nożną, czy jego pasją są szachy, czy jego pasją jest siatkówka, czy pływanie, czy sporty bardziej wymagające powodujące urazy. My powinniśmy to im zapewnić i ich ochronić, w miarę możliwości, przed krwawieniami. Ta indywidualizacja jest takim krokiem dosyć istotnym w kierunku właśnie ochrony danego pacjenta przed krwawieniami” – podkreśla prof. Anna Klukowska. „Powinniśmy dbać o rozwój aktywności u naszych pacjentów, bo przecież dochodzi do wzmocnienia masy mięśniowej, do zabezpieczenia stawów, i co jest ważne, o czym obecnie się niestety mówi w pediatrii, o otyłości u naszych pacjentów, które mają niekorzystny wpływ na rozwój stawów i częstość krwawień” – dodaje prof. Paweł Łaguna. Dzięki nowym narzędziom, aplikacjom na telefon chorzy oraz ich bliscy mają możliwość kontroli obecnego stanu zdrowia oraz doboru odpowiedniej dawki czynnika, również w zależności od potrzeb. „Możemy wyliczyć ten czas, kiedy aktywność czynnika spada zdecydowanie do takich, kiedy należy podać kolejną dawkę. Pacjent po analizie farmakokinetycznej, po ustaleniu częstotliwości podawania ustalonej dawki, otrzymuje kod QR, który może wprowadzić do swojego smartfona. Wprowadzając kolejne podania ma to przełożenie na to, że jest interpretowana i wyświetlana aktualna przybliżona aktywność czynnika VIII” – zaznacza dr Andrzej Kołtan. Edukacja pacjentów w zakresie samodzielnego podawania czynnika, zwłaszcza przy dostępie do najnowszych technologii, odgrywa dziś fundamentalną rolę. „W tej chwili hemofilia jest chorobą, w której pacjent i jego opiekunowie leczą się de facto sami. Robią to w warunkach domowych – do domu dostarczany jest czynnik, sprzęt medyczny. Teraz, jeśli ma to być ta spersonalizowana profilaktyka, to pacjent w określonym momencie czasowym podaje sobie czynnik VIII” – podkreśla prof. Tomasz Urasiński. Specjaliści podczas debaty podkreślili istotną rolę edukacji pacjentów oraz ich opiekunów w zakresie zrozumienia interpretacji farmakokinetyki, na podstawie której istnieje możliwość indywidualnego doboru dawki czynnika VIII oraz jego częstotliwości podania za pomocą aplikacji mobilnych wspierających pacjentów w ich aktywnym życiu. Zachęcamy do obejrzenia I części debaty eksperckiej pt. „Personalizacja profilaktyki hemofilii A – dodatkowe funkcje czynnika VIII. Przyszłość leczenia hemofilii”, podczas której eksperci podzielili się swoją wiedzą dotyczącą roli, jaką odgrywa czynnik VIII w organizmie człowieka i dlaczego jest ważny podczas terapii pacjentów z hemofilią oraz spostrzeżeniami na temat stosowania możliwych terapii w przyszłości. Zapraszamy do obejrzenia nagrania. C-ANPROM/PL/NON/0025 03/2025 Artykuł edukacyjny na podstawie filmu skierowany do szerokiej publiczności przygotowany z inicjatywy i sponsorowany przez Takeda. Wypowiedzi ekspertów bazują na ich wiedzy i doświadczeniu. Przedstawione informacje nie zastępują profesjonalnej porady medycznej. Wszystkie osoby biorące udział w nagraniach wyraziły zgodę na publikację wizerunku. Copyright ©2025 Takeda Pharmaceutical Company Limited. Wszystkie prawa zastrzeżone. Wszystkie znaki handlowe są własnościami ich prawowitych właścicieli. Takeda Pharma sp. z o.o., ul. Prosta 68, 00-838 Warszawa, Polska, telefon: +48 22 608 13 00 lub 01, www.takeda.com/pl-pl

27 lutego 2025
Serdecznie zapraszamy do obejrzenia I części debaty eksperckiej pt. „Personalizacja profilaktyki hemofilii A – dodatkowe funkcje czynnika VIII. Przyszłość leczenia hemofilii”, podczas której eksperci podzielili się swoją wiedzą dotyczącą roli, jaką odgrywa czynnik VIII w organizmie człowieka i dlaczego jest ważny podczas terapii pacjentów z hemofilią oraz spostrzeżeniami na temat stosowania możliwych terapii w przyszłości. https://vimeo.com/1047844735/5e568df274 Dyskusja, poprowadzona przez prof. Pawła Łagunę, kierownika Kliniki Hematologii Dziecięcej i Transplantologii Klinicznej Warszawskiego Uniwersytetu Medycznego, w której udział wzięli prof. Anna Klukowska, prof. Tomasz Urasiński oraz dr Andrzej Kołtan, skupiła się na roli czynnika VIII w hemostazie i jego wpływu na inne procesy w organizmie, takie jak czynność nerek, angiogeneza i modelowanie kości, a także możliwościach leczenia hemofilii A, jakie potencjalnie stosowane będą w przyszłości. „Przyszłość to ciągle jeszcze czynnik VIII rozumiany bardzo szeroko, nawet jeśli rozmawiamy o terapii genowej, to terapia genowa za swój cel ma przywrócenie produkcji prawidłowego czynnika. Więc to jest jednak czynnik, czynnik, czynnik i jeszcze raz czynnik” – podkreśla prof. Tomasz Urasiński. – „Chociaż perspektywa leków nieczynnikowych w tej chwili jest fascynująca, spora część badań obierze kierunek wydłużenia czasu aktywności czynników krzepnięcia, rozumianych jako te fizjologiczne czynniki krzepnięcia, przedłużenia ich działania i zmiany drogi jego podawania” – dodaje Pan profesor. „Patrząc na to, czym w tej chwili dysponujemy w terapiach nieczynnikowych, to cały czas te terapie zamieniają hemofilię ciężką na co najwyżej łagodną. Czyli aktywności, które będą równoważyć aktywności czynnika VIII na poziomie kilkunastu, powiedzmy 20%. Natomiast do aktywności fizycznych, do prowadzenia pełnego życia – gra w piłkę, jakaś ścianka, wspinaczki, potrzeba zdecydowanie więcej” – mówi dr Andrzej Kołtan. „Pojawienie się czynnika VIII o przedłużonym działaniu, gdy ten czas to około pięćdziesiąt, pięćdziesiąt parę godzin, jest już obiecujące, ale oczywiście na jednym czynniku trudno oprzeć leczenie. Myślę, że personalizacja, o której mówiliśmy, jest bardzo istotna. Nie dla wszystkich wszystko będzie odpowiednie. Leczenie, w zależności od trybu życia, od farmakokinetyki, podjętych aktywności grożących urazem, wybierać będzie ten pacjent, początkowo rodzice, później pacjent. A my powinniśmy rzeczowo i w pełni informować rodziców i pacjentów, jakie są możliwości, jakie są korzyści, jakie wady leczenia i wobec tego umożliwić im podjęcie najlepszej decyzji” – zaznacza prof. Anna Klukowska. Eksperci podczas debaty podkreślili znaczenie personalizacji leczenia hemofilii A i konieczności informowania pacjentów oraz rodziców o korzyściach i wadach różnych opcji terapeutycznych. Zaznaczyli, że pomimo niepewnej przyszłości leczenia, rozwój czynników krzepnięcia i terapii nieczynnikowych daje nadzieję na poprawę jakości życia pacjentów. II część debaty eksperckiej pt. „Personalizacja profilaktyki hemofilii A – skuteczność i bezpieczeństwo terapii” zostanie poświęcona omówieniu postępów w leczeniu hemofilii u dzieci, z uwzględnieniem włączenia pacjentów z ciężką postacią hemofilii A i B do profilaktyki. Zapraszamy do obejrzenia nagrania. C-ANPROM/PL/ADV/0029 02/2025 Artykuł edukacyjny na podstawie filmu skierowany do szerokiej publiczności przygotowany z inicjatywy i sponsorowany przez Takeda. Wypowiedzi ekspertów bazują na ich wiedzy i doświadczeniu. Przedstawione informacje nie zastępują profesjonalnej porady medycznej. Wszystkie osoby biorące udział w nagraniach wyraziły zgodę na publikację wizerunku. Copyright ©2024 Takeda Pharmaceutical Company Limited. Wszystkie prawa zastrzeżone. Wszystkie znaki handlowe są własnościami ich prawowitych właścicieli. Takeda Pharma sp. z o.o., ul. Prosta 68, 00-838 Warszawa, Polska, telefon: +48 22 608 13 00 lub 01, www.takeda.com/pl-pl

23 grudnia 2024
Niech rozwiążą się wszystkie zagmatwane sprawy,Niech wszystkie kręte drogi staną się proste,Niech światło będzie potężniejsze od mroku, a ciepło od chłodu,Niech to, co nas łączy, będzie o wiele silniejsze niż to, co dzieli – nie tylko od Święta. Życzy Redakcja Portalu Hemopozytywni.pl.

19 listopada 2024
Zapraszamy do zapoznania się z broszurą autorstwa lek. Anny Badowskiej, dr n. med. Elżbiety Latos-Grażyńskiej i dr. n. med. Grzegorza Dobaczewskiego pt. "Zdrowe stawy w hemofilii. Profilaktyka rehabilitacją". https://issuu.com/hematoonkologia.pl/docs/poradnik_zdrowe-stawy-w-hemofilii W publikacji znaleźć można ogólne informacje o tym, czym jest hemofilia, jak powstaje i w jaki sposób się objawia, a także: jak postępować w przypadku krwawień dostawowych i domięśniowych, na czym polega profilaktyka hemofilii, jak ważna jest aktywność fizyczna dla osób z hemofilią. Ponadto w broszurze opisane zostały przykładowe ćwiczenia odpowiednie dla dzieci z hemofilią, dostosowane do etapu ich rozwoju. Zapraszamy do przeczytania publikacji.

18 listopada 2024
Dzisiaj Jaś ma 10 lat. Ponad 8 lat temu okazało się, że choruje na ciężką postać hemofilii A. Chociaż na początku diagnoza była dla jego rodziny szokująca, teraz chcą oni udowodnić, że z hemofilią można żyć normalnie i spełniać swoje marzenia. https://youtu.be/BAHQcRm3-lI?feature=shared Historia Jasia rozpoczęła się od naderwanego wędzidełka. Był to drobny uraz, ale krwawienie trwało wiele godzin. Po wizycie w szpitalu niepokojące symptomy się jednak spotęgowały, ponieważ mimo że wędzidełko było już zszyte, w miejscach, w których lekarze dotykali chłopca podczas przygotowań do zabiegu oraz w miejscach, gdzie miał założone wenflony, pojawiły się ogromne siniaki. „Ze szpitala w Gorzowie zostaliśmy wypisani do domu, skierowani do poradni hematologicznej w Szczecinie, ale tego samego dnia u Janka pojawiły się już tak ogromne obrzęki, które nie pozwalały mu na to, żeby mógł poruszać szyją, nie pozwalały na to, żeby mógł stanąć na jedną nóżkę i w miejscach, gdzie był zakłuwany, wylewy były tak ogromne, że nie mogliśmy nawet mu ubrać koszulki na ramię” – wspomina pani Dominika, mama Jasia. – „Ze szpitala w Gorzowie zostaliśmy przetransportowani do Szczecina i tam kolejnego dnia padło rozpoznanie. Była to dla nas szokująca diagnoza, natomiast, cofając się w czasie, zauważyłam wiele symptomów, które wskazywałyby na to, że Jasio ma zaburzenia krzepliwości krwi”. Nauka raczkowania, przypadkowe uderzenie w nogę krzesła czy nawet nadgryzienie ust – nawet tak drobne urazy powodowały u chłopca duże siniaki. Diagnoza zmieniła wszystko „W momencie, kiedy Jasio został zdiagnozowany, nasze życie bardzo się zmieniło” – opowiadała mama Jasia, wspominając swoją obawę o to, czy syn przez swoją chorobę będzie akceptowany, czy będzie miał kolegów czy też zostanie odtrącony. – „Z chłopca bardzo aktywnego nagle stał się chłopcem chodzącym z nami za rękę, ale to trwało bardzo krótko”. Wszystko się zmieniło, gdy została wdrożona profilaktyka, a Jasio zaczął regularnie otrzymywać czynnik krzepnięcia. Leczenie dało nadzieję, że to wszystko, co miało być niemożliwe przez hemofilię, stanie się możliwe. „Początki były trudne” Początki leczenia były dla Jasia bardzo trudne i stresujące. „Jasio był pulchnym chłopcem, więc znalezienie żyłek, nawet przez profesjonalne pielęgniarki na oddziale hematologicznym w Szczecinie, było dla nich bardzo trudne” – mówi mama Jasia. Po kilku miesiącach lekarz prowadzący zadecydował jednak o zaimplantowaniu portu dożylnego, dzięki któremu przez 8 lat życia Jasia, podawanie czynnika stało się nieco prostsze. – „Po 8 latach funkcjonowania portu Jasia, przeszliśmy do kolejnego etapu. Kolejnym etapem było pozbycie się portu, usunięcie go. Przeszliśmy na żyłki”. „Samo podanie leku jest proste, to jest niewielka objętość wstrzyknięta w czasie dosłownie 2-3 minut, po czym we krwi stężenie czynnika krzepnięcia błyskawicznie wzrasta do takich wartości, które widzimy u zdrowych ludzi. Więc w tym momencie w cudowny sposób uzdrawiamy to, co nazywamy hemostazą pacjenta. Dzięki temu pacjent wykrzepia w razie urazu tak samo, jak każdy jego zdrowy kolega, rówieśnik” – stwierdza prof. dr hab. n. med. Tomasz Urasiński, Kierownik Kliniki Pediatrii, Hemato-Onkologii i Gastroenterologii Dziecięcej w Szczecinie. „Bo ja generalnie mogę robić wszystko” Chłopiec już wie, co zrobić, żeby podanie czynnika krzepnięcia mogło przebiec jak najsprawniej. „Budzę się, jem śniadanie, ubiorę się i muszę pamiętać o tym, żeby pić wodę przed czynnikiem i być najedzony, bo dzięki temu żyły się bardziej pojawiają i lepiej jest się wkłuć” – wymienia pacjent. – „Mama szykuje czynnik, strzykawki, sól fizjologiczną, tysiączkę i pięćsetkę czynnika do jednej i drugiej strzykawki. No i igłę i kilka gazików. Mama na początek bierze, szuka żył w jednej i drugiej ręce, potem wybiera i kiedy się wkłuje, to musi też pobrać krew, żeby zobaczyć, czy jest wszystko okej, co jakiś czas, tak 30 sekund. Później się podaje na początek sól, żeby przepłukać żyłę i wężyk. Później podajemy czynnik. Są dwie strzykawki i na początek podajemy tą, w której jest więcej czynnika. Czasami mamię podaje sól na koniec, żeby ona mogła szybko wziąć gazik i żeby szybko wyjęła igłę”. Dzięki podaży czynnika Jasio może prowadzić życie dokładnie takie, jak jego zdrowi rówieśnicy. Wyjeżdża na zielone szkoły, uprawia sport. „Jasio podczas lekcji WF-u zapałał miłością do koszykówki. Jeszcze chyba ma takie wspomnienie, że ze swoją panią wychowawczynią Anią również grali w koszykówkę podczas pobytu w ramach świetlicy na boisku. Miał kolegów, którzy grają w koszykówkę, to są jego najlepsi kumple z klasy. No więc Jasiu zaczął z nimi grać i w ten oto sposób narodziła się ta wielka miłość” – opowiada pani Dominika. Jaś już wie, jak może samodzielnie kontrolować poziom czynnika, by móc grać w koszykówkę: – „Korzystam z aplikacji i są różne kolory, na przykład zielony, czerwony i pomarańczowy. Zielony to jest, że mogę uprawiać różne sporty, a czerwony, że trzeba podać kolejny czynnik”. „Pamiętam taki moment przełomowy w moim myśleniu, kiedy jego starsze siostry grały w hokeja i jeździły na łyżwach, on był taki malutki i chodził ze mną na te treningi, obserwował dziewczynki, jak jeżdżą, to takim błagalnym wręcz wzrokiem na mnie spojrzał i mówił: „Mama, powiedz mi, że zapytasz kiedyś doktora, czy ja też będę mógł tak jeździć”. Pamiętam, że to był początek jego choroby, chwila po diagnozie. Ja nie wiedziałam, co mu odpowiedzieć. Natomiast w momencie, kiedy dzisiaj pyta, czy on będzie mógł coś zrobić, ja mówię jasno, oczywiście Jasiu, jak podasz sobie czynnik, będziesz dorosły, będziesz mógł robić wszystko” – wspomina pani Dominika. „Aktywność fizyczna wzmacnia układ mięśniowo-stawowy. Ten układ staje się przez to bardziej odporny na urazy, a dzięki temu zmniejsza się ryzyko krwawień. Tyle tylko, że trzeba się wyrwać z błędnego koła, bo pacjent z ciężką postacią hemofilii nie może ćwiczyć, bo ryzykuje urazy. Ale przerwanie błędnego koła następuje dzięki profilaktyce, bo, podając czynnik, czynimy hemostazę pacjenta zdrową. Może on wykonywać dokładnie to samo, co każdy jego zdrowy kolega. Nam zależy wręcz na tym, żeby dzieci, chłopcy z ciężką postacią hemofilii uprawiali jak najczęściej sport, żeby właśnie wzmacniać aparat mięśniowo-stawowy” – przypomina prof. Urasiński. W drodze do samodzielności Chociaż terapia czynnikiem krzepnięcia może wydawać się bolesna i trudna, może przynieść pacjentom z hemofilią ogromną ulgę oraz sprawić, że ich choroba jest praktycznie niezauważalna. „Święcie wierzę i przekonuję pacjentów do tego, że warto zapłacić cenę, jaką jest ta wielokrotność wstrzyknięć dożylnych po to, żeby ta hemostaza funkcjonowała normalnie, prawidłowo, chroniąc ich przed krwawieniami. Kiedy zaczynałem pracę, a nasi pacjenci, kończąc 18 lat, przechodzili pod opiekę hematologów dorosłych, większość z nich wędrowała tam o kulach albo na wózkach inwalidzkich. Takich widoków już Państwo dzisiaj nie zobaczycie. Ci chłopcy zdrowi, wysportowani, bez ograniczeń ruchowych maszerują do dorosłych hematologów sami, a ci są zdziwieni, a poniekąd i trochę zmartwieni, bo w ten sposób odbieramy im chleb” – podkreśla prof. Urasiński. „Dzisiaj podajemy czynnik razem, natomiast mam nadzieję i cały czas pracujemy nad tym, aby w niedalekiej przyszłości Jasiu był absolutnie samodzielny, jeśli chodzi o podawanie czynnika krzepnięcia” – podkreśla pani Dominika. „Myślę, że w przyszłości, gdzieś za pół roku, będę sobie chyba sam podawać” – przypuszcza Jasio. Artykuł edukacyjny na podstawie filmu skierowany do szerokiej publiczności, przygotowany z inicjatywy i sponsorowany przez Takeda. Przedstawione informacje nie zastępują profesjonalnej porady medycznej. W przypadku jakichkolwiek pytań lub wątpliwości należy skontaktować się z lekarzem. Wszystkie osoby biorące udział w nagraniach wyraziły zgodę na publikacje wizerunku. VV-MEDMAT-113376, 11/2024Copyright © 2024 Takeda Pharmaceutical Company Limited.Wszystkie prawa zastrzeżone. Wszystkie znaki handlowe są własnościami ich prawowitych właścicieli. Takeda Pharma Sp. z o. o.ul. Prosta 68, 00-838 Warszawa, PolskaTel.: +48 22 608 13 00 lub 01www.takeda.com/pl-pl/

16 września 2024
Zapraszamy do zapoznania się z materiałem edukacyjnym dla pacjentów, rodzin i personelu medycznego, prezentującym możliwości, jakie niesie spersonalizowana profilaktyka krwawień.
19 lipca 2024
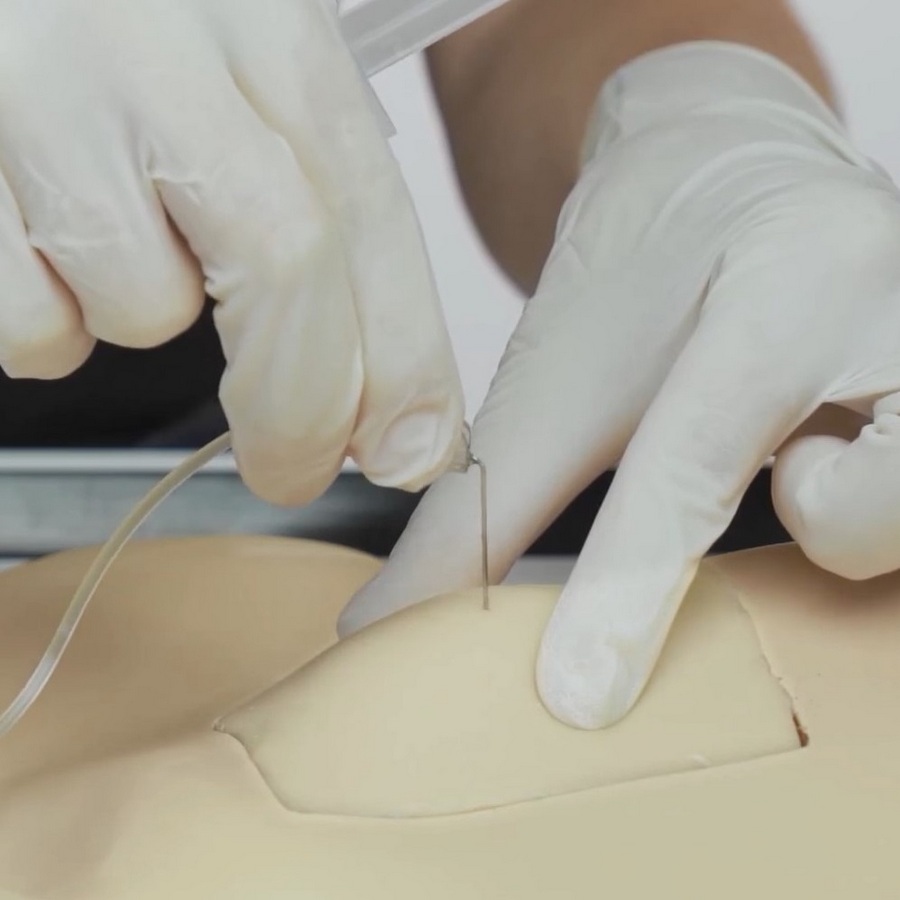
Zapraszamy do zapoznania się z nagraniem, w którym zaprezentowany został prawidłowy sposób opieki nad "portem". W materiale zostało pokazane: przygotowanie do podania czynnika, przygotowanie czynnika i odpowiedniego sprzętu, jak odpowiednio przygotować osobę, której będzie podany czynnik, w jaki sposób prawidłowo podać czynnik za pośrednictwem "portu", jak zakończyć zabieg i zabezpieczyć miejsce wkłucia, jakie są możliwe powikłania związane z używaniem portu dożylnego. https://vimeo.com/985547326 Materiał powstał na zlecenie firmy Takeda.

18 lipca 2024
Zapraszamy do zapoznania się z nagraniem, w którym zaprezentowany został prawidłowy sposób przeprowadzania autoiniekcji. W materiale zostało zaprezentowane: w jaki sposób przygotowania do przeprowadzenia autoiniekcji, w jaki sposób przygotowania leku oraz niezbędnego sprzętu, jakie są zalecane miejsca do dożylnych iniekcji, jakich miejsc należy unikać, co świadczy o prawidłowym wykonaniu iniekcji, w jaki sposób uwidocznić żyłę, jak przeprowadzić autoiniekcję do żyły zgięcia łokciowego oraz autoiniekcję do żyły dłoni. https://vimeo.com/983026185 Materiał powstał na zlecenie firmy Takeda.
12 lipca 2024
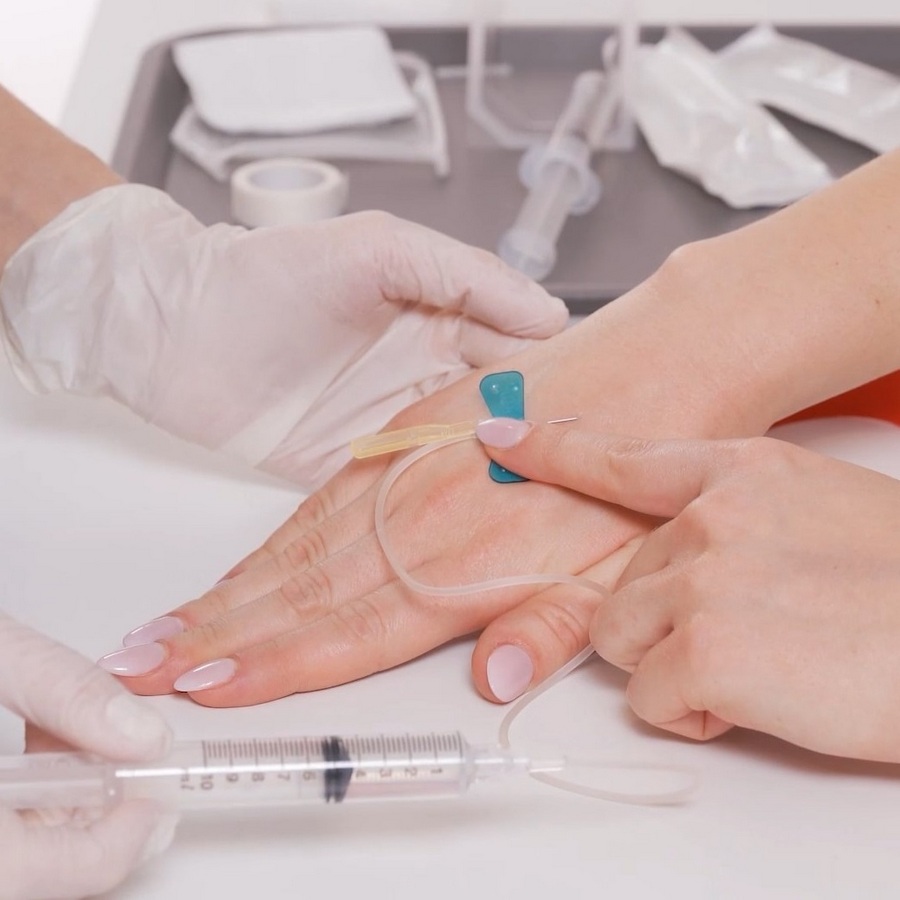
Zapraszamy do zapoznania się z nagraniem, w którym zaprezentowany został prawidłowy sposób przeprowadzania iniekcji. W nagraniu wyjaśnione zostały następujące elementy: sposób przygotowania do przeprowadzenia iniekcji, sposób przygotowania leku i niezbędnego sprzętu, zalecane miejsca do dożylnych iniekcji, jakich miejsc należy unikać, co świadczy o prawidłowym wykonaniu iniekcji, sposoby na uwidocznienie żyły, jak wygląda iniekcja do żyły dłoni oraz żyły zgięcia łokciowego. https://vimeo.com/983026076 Zapraszamy do zapoznania się z materiałem. Materiał powstał na zlecenie firmy Takeda.

14 czerwca 2024
“Sądzę, że każdy z nas ma swoją własną „hemofilię” w życiu – trudność, która wydaje się nie do pokonania. Sposób, w jaki poradzimy sobie z tym wyzwaniem będzie określał dokąd ostatecznie dojdziemy w życiu” – Adam Trojańczyk. „Życie jest jak pudełko czekoladek – nigdy nie wiesz, co Ci się trafi” to słowa wypowiadane przez Foresta Gumpa, bohatera książki Winstona Grooma, które weszły do kanonu bon mot dzięki ekranizacji powieści i genialnej roli Toma Hanksa. Są one symbolem zmagań osób na co dzień borykających się z wszelkimi chorobami. Niekiedy niektórzy z nas dostają od życia coś czego nie planowali, np. chorobę przewlekłą. Życie wtedy staje się nie lada wyzwaniem. Jednak, mimo wielu trudności i obciążeń jakie niesie ze sobą choroba, można realizować swoje cele i nie rezygnować z marzeń. Przydaje się do tego siła charakteru, determinacja i bardzo ważny element życia – wsparcie najbliższych. Forest Gump, dotknięty autyzmem, biegł przez Stany, by ukoić ból spowodowany odrzuceniem miłosnym. Terry Fox, 22-letni Kanadyjczyk, który mógłby być pierwowzorem bohatera książki i filmu biegł po amputacji prawej nogi, by zwiększyć świadomość Kanadyjczyków na temat chorób nowotworowych. Adam Trojańczyk ćwiczy, strzela i dzieli się swoimi doświadczeniami życia z hemofilią typu B. Historia Adama Trojańczyka, 39 latka, który od urodzenia stawia czoła hemofilii jest opowieścią o człowieku, który mimo wielu trudności i przeciwności losu zdecydował, że chce walczyć o siebie i swoją pogodną przyszłość. Gdy po latach okazało się, że osiągnął swój szeroko rozumiany sukces, jego wrażliwość pchnęła go o krok dalej. Postanowił, że przełamie jeszcze jedno swoje ograniczenie – poczucie wstydu i skrępowania i zacznie dzielić się swoją historią z innymi. Jego celem jest zarażanie ludzi optymizmem. Obecnie jest odnoszącym sukcesy CEO, ale przede wszystkim stał się rzecznikiem osób, które zmagają się z chorobami przewlekłymi. Mamy nadzieję, że historia Adama będzie dla was inspiracją i pozwoli wam budować waszą historię, która być może pewnego dnia stanie się ważna dla kogoś innego. Choroba Osoba, która od urodzenia żyje z ostrą formą hemofilii typu B jest mocno doświadczona, zahartowana i wytrenowana do stawiania czoła wszelkim przeciwnościom losu. Trudności związane z chorobą, częstymi hospitalizacjami, rozłąkami z rodzicami, bólem wynikającym z nieustannych zabiegów medycznych, wkłuć, pobierania krwi w tak młodym wieku mogłyby sugerować, że jedyne na co może sobie pozwolić osoba z hemofilią to niezbędny sen i odpoczynek, aby zebrać siły na kolejny dzień walki. Historia Adama pokazuje nam wszystkim, że tak nie jest i zachęca innych, by brali z niego przykład. Adam jest mężczyzną, mężem i ojcem, ambitnym, pełnym pasji, niezmiernie wrażliwym, osiągającym sukcesy zawodowe, sumiennym, bardzo pracowitym i wysportowanym. Życie Adama od samego początku było zagrożone z uwagi na możliwość wystąpienia trudnych do opanowania krwawień wewnętrznych. „Pierwsze krwawienie wystąpiło u mnie, zaraz po moich pierwszych urodzinach. Gdy byłem dzieckiem, rodzice stale walczyli o moje zdrowie, a nasze życie było przerywane częstymi wizytami w szpitalu. Było ich tak wiele, że gdy teraz o nich myślę, to zlewają mi się w pamięci w jeden ciągły pobyt szpitalny.” W wyniku krwawień w jego nogach wystąpiły zatory, które doprowadziły do całkowitego zaniku mięśni, atrofii, a ból towarzyszył mu praktycznie w każdej minucie życia. Nawet w tak trudnej chwili, Adam nie poddał się i wykazał się ogromną siłą charakteru. Za wszelką cenę chciał powrócić do formy, odzyskać sprawność w nogach i ponownie normalnie funkcjonować. „Zdeterminowany, aby poprawić moją kondycję fizyczną, rozpocząłem przygodę z treningami sportowymi. Na początku mojej drogi, przez pierwszych kilka lat, pojawiałem się na siłowni pięć razy w tygodniu”. Dzięki ćwiczeniom wykorzystującym masę ciała osoby trenującej, kalistenice oraz taśmie TRX Adam wrócił do pełni sił. W ciągu ośmiu lat wykonał około 3000 sesji treningowych, dzięki czemu udało mu się pozbyć większości przykurczy w stawach, przestał kuleć i zauważył znaczące zmiany w swoim ogólnym funkcjonowaniu. Rodzice Gdy na chorobę przewlekłą choruje dziecko to tak naprawdę choruje cała rodzina. Każdy przeżywa tę sytuację w inny sposób. Inaczej interpretuje ją i przeżywa chore dziecko, rodzeństwo, rodzice czy dziadkowie. To przede wszystkim rodzice chorych dzieci stawiani są przed ogromnym wyzwaniem, zarówno fizycznym jak i psychicznym. Świadomość, że ukochane dziecko od początku życia będzie borykać się z trudnościami i bólem jest bardzo wyczerpująca. Ale równie wyczerpujące jest żonglowanie domem, pracą, szpitalem, snem, własnymi pasjami i czasem wolnym. Trudno jest to wytłumaczyć osobom, które nie doświadczyły momentu przyjmowania informacji o diagnozie swojego dziecka. Rodzice dzieci przewlekle chorych są cichymi bohaterami, nad którymi powinno się roztaczać szczególną opiekę. Zasługują na szacunek, podziw, pomoc i wyrozumiałość. „W wyniku masywnego krwawienia do kolana przestałem chodzić. Przez kilka miesięcy leżałem w szpitalu oddalonym o setki kilometrów od naszego domu rodzinnego. Mój tata odwiedzał mnie codziennie. Przyjeżdżał pociągiem po pracy, by spędzić ze mną trochę czasu. Do domu wracał późno w nocy, chwilę drzemał i o 4 nad ranem wstawał, by znowu zdążyć do pracy. Imponował mi swoją postawą i determinacją, a także nauczył jaką dużą wartość ma miłość zbudowana na zaangażowaniu i poświęceniu dla drugiej osoby. To dzięki tacie, sam stałem się oddanym ojcem dla moich dzieci”. Przekuwanie przeciwności losu w sukces Arystoteles pisał, że ten kto nie czerpie przyjemności z tego co robi i nie odnosi sukcesów, nie może być szczęśliwy. Idąc tym tropem można wnioskować, że każdy kto zajmie się tym co naprawdę sprawia mu przyjemność powinien odnosić sukcesy, być szczęśliwym i dzięki temu obdarowywać szczęściem osoby wokół siebie. Adam z pewnością udowadnia, że jeśli działamy w obszarze, który nas interesuje, w pełni mu się poświęcamy i konsekwentnie dążymy do celu to mimo przeciwności losu nasze działanie doprowadzi nas do sukcesu i szczęścia. „Jako nastolatek interesowałem się wieloma rzeczami. Nocami pisałem wiersze, które były czytane w nocnych programach lokalnej rozgłośni radiowej. W ciągu dnia tworzyłem programy komputerowe. Pierwszy napisałem w wieku 11 lat na Commodore 64. Bardzo polubiłem także matematykę i fizykę, i godzinami rozwiązywałem równania, albo pisałem oprogramowania, które rozwiązywały je za mnie. Moje zamiłowanie do komputerów zaprowadziło mnie na Politechnikę, gdzie studiowałem na Wydziale Fizyki Technicznej, Informatyki i Matematyki Stosowanej. Napędzany nieprzemijającą potrzebą rozwoju bardzo szybko otworzyłem swoją firmę, mimo że byłem totalnie bez grosza. W ten oto sposób od 2004 roku jestem powiązany z branżą IT”. Adam jako młody nastolatek, z uwagi na konieczność oszczędzania się, zmuszony był do przejścia w tryb edukacji domowej. Nie stracił jednak pozytywnego nastawienia do życia. Przez chwilę doświadczał izolacji i osamotnienia, czuł się nieobecny i obciążony, ale jak mówi w wywiadzie przeprowadzonym przez EHC – „Moje doświadczenie związane z chorobą i cierpieniem stało się katalizatorem zmian, zmusiło mnie do jeszcze większej dyscypliny, sumienności i zaprowadzenia porządku w moim życiu. Te wartości przyświecają mi w życiu i pomagają nie ustawać w działaniu, mimo trudności, które napotykam. Moja determinacja sprawia, że nigdy się nie poddaję”. Obecnie jest dyrektorem generalnym w firmie tworzącej oprogramowanie. Jego działania na rzecz osób chorujących na hemofilię sprawiły, że w 2019 roku został wybrany na członka głównego Zarządu Polskiego Stowarzyszenia Chorych na Hemofilię, a w 2023 roku został Prezesem Koła PSCH w Łodzi. Doświadczenie choroby, ból i cierpienie, postawa i opieka rodziców ukształtowały jego silny charakter. – „Nauczyłem się jak prowadzić firmę, dokładnie w ten sam sposób, w jaki nauczyłem się samodzielnie wstrzykiwać lek. Zacząłem od początku i wyciągałem wnioski z popełnianych błędów”. Wartości, którymi kieruje się w życiu, takie jak potrzeba samorozwoju, zmieniania świata na lepsze i altruizm, ukształtowały człowieka sukcesu, jakim niewątpliwie jest Adam Trojańczyk. To co wyróżnia Adama spośród większości ludzi to ogromna szczerość i otwartość w sposobie mówienia o chorobie. Adam bez wahania przyznaje jak trudno było mu otworzyć się i z odwagą, i z godnością opowiadać o swojej niełatwej historii z chorobą w tle. Adam podkreśla, że do działania i jeszcze większego zaangażowania w sprawy chorych na hemofilię motywuje go żona oraz wiadomości spływające od osób, z którymi spotyka się podczas prelekcji, spotkań na uniwersytetach czy tych organizowanych w miastach przy okazji dni świadomości hemofilii. Bardzo istotnym przekazem Adama, zwłaszcza do młodych osób jest zwrócenie uwagi na fakt, iż: “W czasach mediów społecznościowych obserwujemy zniekształconą rzeczywistość pokazującą same dobre momenty życia, pięknych, zdrowych ludzi i natychmiastowe wyniki działań. Za mało mówimy o wyzwaniach życia codziennego i motywacji niezbędnej do naszego rozwoju. Zdałem sobie sprawę, że wyjście z cienia i mówienie otwarcie o swoich trudnościach i problemach może być ratunkiem dla kogoś w potrzebie i inspiracją do zmiany życia na lepsze”. Źródło: ehc.eu
13 kwietnia 2024
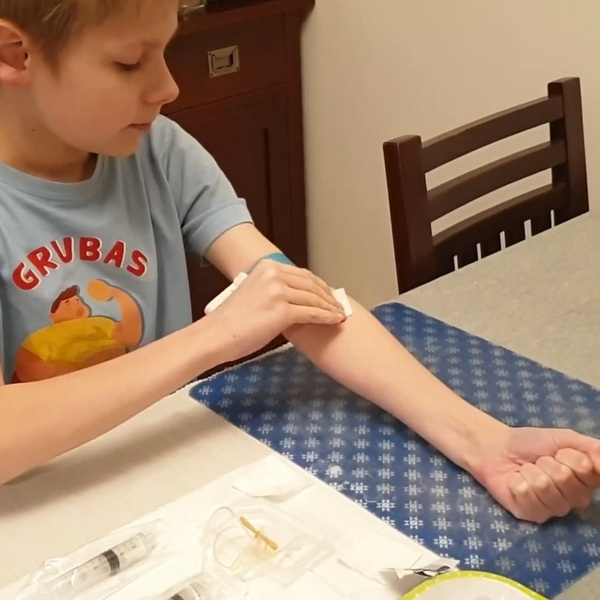
Zapraszamy do zapoznania się z filmami, w których zaprezentowane zostały przyjazne metody podawania czynnika krzepnięcia u małych dzieci oraz autoiniekcją u starszych dzieci.Bohaterem filmów jest Gucio oraz jego historia podawania czynnika krzepnięcia na przestrzeni kilku lat. https://www.youtube.com/watch?v=ZsHweS0TKOM https://youtu.be/NQe3vtR5zDY?feature=shared Zapraszamy do zapoznania się z materiałami.

28 marca 2024
Szanowni Państwo, z okazji zbliżających się Świąt Wielkanocnych życzymy radości, życzliwości i nadziei. Niech ten czas przyniesie wytchnienie od codziennych trudów i problemów oraz będzie wyjątkową okazją do spotkania w gronie najbliższych.

22 grudnia 2023
Z okazji zbliżających się Świąt Bożego Narodzenia pragniemy złożyć Państwu serdeczne życzenia zdrowia i radości. Niech ten szczególny czas będzie wypełniony nadzieją i wsparciem najbliższych oraz da wytchnienie od codziennych obowiązków i zmartwień, a Nowy Rok 2024 niech przyniesie wszelką pomyślność. Wszystkiego, co najlepsze!
10 października 2023
W Polsce zespół ekspertów opracował wytyczne postępowania w hemofilii A i B powikłanej i niepowikłanej inhibitorem, które zostały zaktualizowane w 2016 i 2017 roku. Zalecenia dotyczą diagnostyki i leczenia skaz krwotocznych, postępowania z nosicielkami hemofilii, zasad wykonywania badań prenatalnych, strategii postępowania z chorymi na hemofilię. Leczenie chorych z hemofilią powikłaną inhibitorem jest zupełnie inne niż pacjentów bez inhibitora i o tym należy pamiętać. Jeśli u chorego pojawi się inhibitor do czynnika krzepnięcia, wówczas leczenie substytucyjne brakującym czynnikiem krzepnięcia będzie już nieskuteczne. Niezwykle istotne jest wykonywanie regularnie badań na obecność inhibitora do czynnika krzepnięcia przez pacjentów leczonych substytucyjnie, w szczególności chorujących na ciężką postać hemofilii. Co ważne, ryzyko powstania inhibitora jest najwyższe w ciągu 50 pierwszych dni ekspozycji na czynnik krzepnięcia, czyli u najmłodszych chorych, ale wzrasta także u osób starszych. Długość życia chorych na hemofilię wydłuża się dzięki stosowaniu skutecznego leczenia, a starszy wiek predysponuje do chorób cywilizacyjnych, nowotworów i chorzy poszukują pomocy specjalistów. Ośrodki Leczenia Hemofilii, które powstały, powinny nie tylko prowadzić leczenie skaz krwotocznych, ale też umożliwić chorym dostęp do różnych specjalistów. Nadrzędnym celem w postępowaniu z chorym na ciężką hemofilię powinno być efektywne zapobieganie samoistnym krwawieniom do stawów i mięśni oraz krwawieniom zagrażającym życiu, w tym krwawieniom śródczaszkowym, krwawieniom w okresie okołooperacyjnym, a także skuteczne leczenie ostrych epizodów krwawień. Podawanie czynników krzepnięcia w celu zapobiegania krwawieniom określa się mianem profilaktyki, a leczenie epizodów krwawień to leczenie na żądanie (on demand). Podstawą nowoczesnego leczenia hemofilii jest długoterminowa profilaktyka krwawień, rozpoczęta w pierwszych latach życia. W Polsce w 2008 roku wdrożony został program lekowy finansowany przez NFZ o nazwie: „Zapobieganie krwawieniom u dzieci z hemofilią A i B”. Do programu mogły być włączone, za zgodą rodziców, wszystkie dzieci z ciężką postacią hemofilii A i B od urodzenia do ukończenia 18. roku życia, a także dzieci z hemofilią umiarkowaną, jeśli występowały u nich krwawienia dostawowe. Standardowo do programu włączane były dzieci pomiędzy 1. a 2. rokiem życia, u których nie było jeszcze krwawień (lub było jedno krwawienie do stawu), a stosowana profilaktyka nosiła nazwę profilaktyki pierwotnej. Jeśli u pacjentów były wcześniej co najmniej dwa krwawienia do stawów, to włączani byli do profilaktyki wtórnej. Do profilaktyki pierwotnej i wtórnej początkowo stosowano jedynie osoczopochodne czynniki krzepnięcia, z czasem dla nowo włączanych do profilaktyki pacjentów dostępne już były rekombinowane czynniki krzepnięcia. Dawkowanie czynnika krzepnięcia do profilaktyki było stałe, pacjenci mogli otrzymywać w hemofilii A czynnik VIII maksymalnie 3 razy w tygodniu w dawkach od 25 do 40 j./kg. Tak prowadzona profilaktyka nie zawsze była skuteczna. U dzieci zdarzały się krwawienia dostawowe, najczęściej po urazach i konieczne było dodatkowo leczenie krwawień. W ostatnich latach zaszły spore zmiany w programie lekowym, bardzo korzystne dla pacjentów. U dzieci wprowadzono profilaktykę spersonalizowaną opartą o wyniki badań farmakokinetycznych dla stosowanych leków i zależną od potrzeb pacjenta. Pacjenci mogą otrzymywać profilaktycznie czynniki krzepnięcia co drugi dzień, a jeśli jest taka potrzeba, to nawet codziennie, stosowane dawki leków też mogą być zmienne. Spersonalizowana profilaktyka dostosowana do potrzeb chorych, ich aktywności i potrzeb spowodowała zmniejszenie ilości krwawień i polepszenie stanu stawów. Należy jednak pamiętać, że nawet najlepiej ustawione leczenie może być nieskuteczne, jeśli chory nie będzie przestrzegał zaleceń lekarskich. W przypadku dzieci i młodzieży bardzo ważne jest, żeby czynniki krzepnięcia podawać w godzinach rannych, aby wykorzystać ich potencjał. Niestety dość często z powodu braku czasu rodzice podają dzieciom lek po południu lub wieczorem, co powoduje, że maksymalne stężenie leku osiągane jest w godzinach nocnych, kiedy dziecko jest nieaktywne. Koncepcja długoterminowej profilaktyki dostosowanej do indywidualnych parametrów farmakokinetycznych i indywidualnych potrzeb pacjenta służy realizacji najbardziej ambitnego celu w terapii substytucyjnej hemofilii, czyli całkowitego wyeliminowania samoistnych krwawień przy równoczesnej optymalizacji zużycia koncentratów i minimalizowaniu częstości wstrzyknięć dożylnych. Miernikiem skuteczności długoterminowej profilaktyki jest brak krwawień i brak zmian zwyrodnieniowych w stawach ocenianych zarówno w badaniu fizykalnym (wg skali HJHS), jak również za pomocą technik obrazowych. Inny rodzaj profilaktyki to profilaktyka trzeciorzędowa. Polega ona na profilaktycznym podawaniu czynników krzepnięcia regularnie i długoterminowo u chorych, którzy mają udokumentowane zmiany zwyrodnieniowe w stawach. Z kolei profilaktyka okresowa polega na podawaniu czynnika krzepnięcia w celach profilaktycznych przez czas krótszy niż 45 tygodni w roku. Poniżej znajduje się 16 wytycznych długoterminowej profilaktyki krwawień opracowanych przez zespół polskich ekspertów, które są niezwykle ważne i w całości chciałabym je przedstawić. U każdego pacjenta z ciężką hemofilią A lub B należy dążyć do zastosowania pierwotnej profilaktyki krwawień. U każdego pacjenta z ciężką hemofilią A lub B, u którego nie zastosowano pierwotnej profilaktyki krwawień, należy dążyć do zastosowania profilaktyki wtórnej. U każdego chorego na ciężką hemofilię A lub B z artropatią hemofilową, należy rozważyć zastosowanie trzeciorzędowej profilaktyki krwawień. U części pacjentów objętych długoterminową profilaktyką krwawień, u których nie występują żadne samoistne krwawienia i których fenotyp krwotoczny określa się jako łagodny, można rozważyć zakończenie regularnego wstrzykiwania koncentratu niedoborowego czynnika krzepnięcia z chwilą osiągnięcia dojrzałości fizycznej. U pacjentów takich należy stosować okresową profilaktykę krwawień w sytuacjach zwiększonej aktywności fizycznej, kiedy ryzyko wystąpienia krwawień zwiększa się. Jeśli po zakończeniu długoterminowej profilaktyki zaczynają pojawiać się krwawienia do stawów lub o innym umiejscowieniu, należy powrócić do regularnego wstrzykiwania koncentratu niedoborowego czynnika krzepnięcia. Powrót do długoterminowej profilaktyki jest szczególnie wskazany, gdy krwawienia uniemożliwiają kontynuowanie edukacji lub podjęcie pracy zawodowej. Dane z piśmiennictwa nie pozwalają na określenie optymalnych dawek FVIII i FIX w ramach długoterminowej profilaktyki. Za najbardziej właściwe uważa się: w hemofilii A: podawanie FVIII w dawce 25-50 IU/kg 3 razy w tygodniu lub co drugi dzień, w hemofilii B: podawanie FIX w dawce 25-50 IU/kg 2 razy w tygodniu (ze względu na różnice właściwości farmakokinetycznych pdFIX i rFIX, dawki rFIX mogą być większe niż pdFIX), u części pacjentów dobry efekt kliniczny osiąga się po zastosowaniu mniejszych dawek i/lub wydłużając odstępy między iniekcjami. Jednakże część pacjentów będzie wymagała większych dawek lub ich częstszego podawania. Koncentrat niedoborowego czynnika krzepnięcia powinien być podawany rano, a nie wieczorem przed snem (szczyt aktywności czynnika krzepnięcia powinien przypadać w ciągu dnia). Jeśli w trakcie stosowania długoterminowej profilaktyki pojawiają się krwawienia, należy rozważyć zmianę schematu profilaktyki (np. zmniejszenie odstępów między wstrzyknięciami albo zastosowanie dodatkowych wstrzyknięć, np. przed okresami zwiększonej aktywności fizycznej). Krwawienia występujące w okresie profilaktyki leczy się w taki sam sposób, jak krwawienia u pacjentów nieobjętych profilaktyką. Częste krwawienia w trakcie długoterminowej profilaktyki świadczą o braku skuteczności zastosowanej formy terapii i są wskazaniem do modyfikacji schematu profilaktycznego. Dodatkowo, należy w takiej sytuacji upewnić się, że nie doszło do pojawienia się inhibitora do niedoborowego czynnika krzepnięcia. Za najbardziej właściwą formę długoterminowej profilaktyki uważa się profilaktykę dostosowaną do indywidualnych potrzeb pacjenta, które wynikają z właściwości farmakokinetycznych niedoborowego czynnika krzepnięcia oraz wieku, dostępu do żył, trybu życia i aktywności fizycznej danego pacjenta. Sposób prowadzenia długoterminowej profilaktyki może ulegać modyfikacjom w przypadku zmian ww. parametrów. Decyzję o rozpoczęciu pierwotnej lub wtórnej profilaktyki, wyborze dawki czynnika VIII lub IX, założeniu cewnika do centralnej żyły podejmuje doświadczony klinicysta z ośrodka leczenia hemofilii. W czasie stosowania pierwotnej i wtórnej profilaktyki pacjenci powinni być poddawani regularnym (nie rzadziej niż co 6-12 miesięcy) badaniom w ośrodkach leczenia hemofilii w celu oceny skuteczności i bezpieczeństwa stosowanego leczenia: oceniać stan narządu ruchu badaniem fizykalnym; zaleca się stosowanie skali HJHS, notować wszystkie epizody krwawień w trakcie stosowania profilaktyki oraz analizować ich potencjalne przyczyny, tak aby modyfikując schemat profilaktyki, można było skuteczniej im zapobiegać, oceniać stosowanie się pacjenta (rodziców pacjenta) do wymogów schematu profilaktyki; nieprzestrzeganie zasad profilaktyki może być przyczyną jej nieskuteczności, okresowo oceniać najniższą aktywność niedoborowego czynnika krzepnięcia w osoczu pacjenta poddawanego długoterminowej profilaktyce; występowanie krwawień i stwierdzenie aktywności niedoborowego czynnika krzepnięcia poniżej <1% jest wskazaniem do modyfikacji programu profilaktyki, rozważyć okresową ocenę stanu narządu ruchu metodami radiologicznymi (MRI w celu poszukiwania niewielkich zmian zwyrodnieniowych); RTG u pacjentów z jawną klinicznie artropatią. Nowoczesne leczenie hemofilii, niezależnie od tego, czy polega na profilaktyce, czy na stosowaniu koncentratów w trybie „na żądanie”, opiera się na terapii domowej. Początkowo rodzice, a następnie sami pacjenci powinni nabyć umiejętności wykonywania dożylnych wstrzyknięć koncentratów czynników krzepnięcia. W przypadku często nawracających krwawień do określonego stawu lub mięśnia u pacjenta z hemofilią A lub B nieobjętego pierwotną, wtórną ani trzeciorzędową profilaktyką należy zastosować przez kilka tygodni lub miesięcy regularne wstrzyknięcia FVIII lub FIX w celu zahamowania krwawień. W okresie krótkoterminowej profilaktyki należy stosować fizjoterapię, która przyspiesza powrót do zdrowia. Dodatkowo należy poinstruować pacjenta, że optymalnym postępowaniem może być rozpoczęcie długoterminowej profilaktyki krwawień. U każdego pacjenta z ciężką hemofilią A lub B, który przebył krwawienie zagrażające życiu (np. do centralnego układu nerwowego), należy rozważyć bezterminową profilaktykę z zastosowaniem koncentratu FVIII lub FIX. Z chwilą wprowadzenia do lecznictwa w Polsce koncentratów czynników krzepnięcia o przedłużonym działaniu, Grupa ds. Hemostazy ogłosi swoje stanowisko w sprawie ich wykorzystania w długoterminowej profilaktyce krwawień u chorych na hemofilię A i B. Leczenie krwawień w hemofilii u chorych może wymagać hospitalizacji. Krwawienia do mięśni i stawów można z powodzeniem leczyć w domu, o ile nie towarzyszy im silny ból. Krwawienia zagrażające życiu muszą być leczone w warunkach szpitalnych. Dawkowanie czynnika VIII lub IX w leczeniu różnych krwawień jest różne. Należy pamiętać, że koncentraty czynników krzepnięcia powinny być wstrzyknięte jak najszybciej po wystąpieniu krwawienia. Pacjent z krwawieniem niepoddającym się leczeniu w warunkach domowych, krwawieniem zagrażającym życiu lub wiążącym się z silnym bólem lub urazem, o dużym nasileniu, a zwłaszcza zlokalizowanym w obrębie głowy, szyi, klatki piersiowej i jamy brzusznej musi być hospitalizowany. Leczenie substytucyjne ciężkich krwawień należy monitorować, oznaczając aktywność niedoborowego czynnika krzepnięcia, a w przypadku słabej reakcji na leczenie konieczne jest wykonanie badania w kierunku inhibitora do czynnika VIII lub IX. U pacjentów ze skazami krwotocznymi zaleca się unikanie zastrzyków domięśniowych oraz leków upośledzających hemostazę, w tym leków antyagregacyjnych i przeciwkrzepliwych. W przypadku ostrego krwawienia do stawów i mięśni za wyjątkiem mięśnia biodrowo-lędźwiowego zalecana aktywność czynnika krzepnięcia powinna wynosić 40-60%. W hemofilii A należy podać czynnik VIII w dawce 20-30 j./kg, w hemofilii B czynnik IX w dawce 60-60 j./kg. Jeśli krwawienie nie ustępuje po 12-24 godzinach (z reguły po 1-2 dawkach koncentratu), pacjent powinien zostać zbadany przez lekarza. W przypadku krwawienia do stawu od lat obowiązuje zasada R.I.C.E (Rest, czyli odpoczynek; Ice, czyli lód; Compression, czyli ucisk; Elevation, czyli uniesienie kończyny). W ostatnim czasie zaczęto jednak podważać zasadność stosowania lodu, ponieważ obniżanie temperatury ciała negatywnie wpływa na proces krzepnięcia krwi i może nasilić krwawienie. Przeciwbólowo można stosować COX-2 inhibitory, paracetamol, a w szczególnych przypadkach leki narkotyczne (lek z wyboru to tramadol). Fizjoterapia powinna być wdrożona z chwilą ustępowania bólu i obrzęku. Jeśli krwawienie nie ustępuje w ciągu 48-72 godzin i towarzyszy mu utrzymujący się ból i obrzęk, wówczas można rozważyć aspirację krwi ze stawu pod osłoną leczenia substytucyjnego. Po aspiracji staw musi być całkowicie unieruchomiony, a aktywność czynnika VIII i IX utrzymywana na poziomie 40-60% przez kolejne 2-3 doby. W każdym przypadku krwawienia do stawu niereagującego na leczenie substytucyjne konieczne jest wykonanie badania na obecność inhibitora. Krwawienia do mięśni mogą być bardzo groźne, krwiaki uciskające na naczynia i nerwy mogą spowodować trwałe uszkodzenia. Krwawienie do mięśnia biodrowo-lędźwiowego może dawać takie same objawy, jak zapalenie wyrostka robaczkowego. Leczenie jest zasadniczo różne, krwawienie do mięśnia leczy się zachowawczo, a zapalenie wyrostka robaczkowego wymaga interwencji chirurgicznej. W leczeniu substytucyjnym krwawienia do mięśnia biodrowo-lędźwiowego stosuje się czynniki krzepnięcia przez wiele dni oraz leki przeciwbólowe, należy odciążać bolący mięsień, stosując odpowiednie ułożenie kończyny, a po ustąpieniu objawów natychmiast rozpocząć rehabilitację. W przypadku podejrzenia krwawienia do centralnego układu nerwowego obowiązuje zasada – najpierw lecz, potem diagnozuj. Urazy głowy należy leczyć substytucyjnie, tak samo intensywnie, jak wylewy krwi do CUN, chyba, że badania obrazowe (tomografia komputerowa, rezonans magnetyczny) wykluczą obecność ostrego krwawienia do mózgu lub rdzenia kręgowego. Konieczne jest uzupełnienie niedoborowego czynnika krzepnięcia jak najszybciej do 100% (czynnik VIII – 50 j./kg; czynnik IX – 100 j./kg). Każdy pacjent z podejrzeniem krwawienia do CUN musi być leczony w warunkach szpitalnych. Pierwszym objawem krwawienia do CUN u chorych z hemofilią są silne bóle głowy. U każdego chorego po przebytym krwawieniu do CUN musi być rozważona bezterminowa wtórna profilaktyka krwawień. Krwawienie do szyi i gardła jest stanem zagrożenia życia z uwagi na ryzyko niedrożności dróg oddechowych. Konieczne jest jak najszybsze wstrzyknięcie czynnika krzepnięcia. Niedoborowy czynnik krzepnięcia należy uzupełnić do 100% normy. Leczenie musi być prowadzone w warunkach szpitalnych, niekiedy w oddziale intensywnej opieki medycznej. Ostry krwotok z górnego odcinka przewodu pokarmowego wymaga leczenia w warunkach szpitalnych i substytucji czynnikiem krzepnięcia. Konieczne może być badanie endoskopowe, aby sprawdzić przyczynę krwawienia i zamknąć krwawiące naczynie. Krwawienie z przewodu pokarmowego powinno być, oprócz substytucji czynnikiem krzepnięcia, leczone lekami hamującymi fibrynolizę (kwas traneksamowy). Krwawienie do gałki ocznej wymaga natychmiastowego podania czynnika krzepnięcia, hospitalizacji i pilnej konsultacji okulistycznej, aby uzyskać opinię o właściwym sposobie dalszego postępowania. W przypadku krwiomoczu, jeśli nie towarzyszy mu ból, postępowanie ogranicza się do leżenia w łóżku i intensywnego nawadniania przez 48 godzin. Jeśli krwiomocz jest bardzo intensywny lub towarzyszy mu ból, konieczne jest rozpoczęcie leczenia substytucyjnego. Jeśli krwiomocz nawraca lub stale występuje krwinkomocz, konieczna jest konsultacja urologa i/lub nefrologa. Krwawienia z błony śluzowej jamy ustnej i krwawienia z nosa można opanować, stosując jedynie leki antyfibrynolityczne (kwas traneksamowy). W przypadku krwawienia z jamy ustnej, lek antyfibrynolityczny może być stosowany miejscowo w postaci roztworu do płukania. Jeśli takie postępowanie nie jest wystarczające, wówczas konieczne jest podanie czynnika krzepnięcia. W krwawieniach z nosa często miejscowo stosuje się spongostan nasączony trombiną oraz ucisk przewodu nosowego. Jeśli krwawienia nawracają, konieczna jest konsultacja laryngologa lub stomatologa. Niewielkie rany i otarcia nie wymagają leczenia substytucyjnego. Ranę należy odkazić i zabezpieczyć plastrem z jałowym opatrunkiem. Tylko głębokie rany wymagają leczenia substytucyjnego. Złamania kości zawsze wymagają leczenia szpitalnego. Pierwszą czynnością jest podanie niedoborowego czynnika krzepnięcia. Wybór dalszego leczenia należy do ortopedy, który zadecyduje o leczeniu operacyjnym lub zachowawczym. Należy unikać długotrwałego unieruchomienia i jak najszybciej rozpoczynać fizjoterapię. Ciąża i poród u kobiety nosicielki hemofilii wymaga nadzoru nie tylko ginekologa, ale też hematologa i genetyka. W czasie ciąży u kobiet nosicielek hemofilii A bardzo rzadko dochodzi do krwawień, ponieważ w okresie ciąży aktywność czynnika VIII wzrasta. Poród powinien się odbywać w ośrodku, który ma dostęp do laboratorium oznaczającego czynniki krzepnięcia oraz do czynników krzepnięcia. W okresie porodu i połogu aktywność czynnika krzepnięcia VIII i IX powinna być utrzymywana powyżej 50%. Sposób porodu powinien być ustalony w oparciu o czynniki położnicze i hematologiczne. W trakcie porodu nie wolno stosować kleszczy ani próżnociągu, ponieważ zwiększa to ryzyko urazu dziecka. Zaleca się, aby badanie aktywności czynników krzepnięcia wykonać z krwi pępowinowej, a każdy noworodek płci męskiej z podejrzeniem lub rozpoznaną hemofilią powinien mieć wykonane przezciemiączkowe USG przed wypisem do domu. W razie stwierdzenia krwawienia, powinien być natychmiast leczony rekombinowanym czynnikiem VIII lub IX. Zabiegi operacyjne u chorych na hemofilię powinny być wykonywane w specjalistycznych centrach leczenia hemofilii, które mają dostęp do odpowiednich koncentratów czynników krzepnięcia i odpowiedniej bazy diagnostycznej. Stosowanie leczenia substytucyjnego w okresie okołooperacyjnym wymaga oznaczania aktywności niedoborowych czynników krzepnięcia w celu stosowania właściwych dawek leków. W przypadku dużych zabiegów operacyjnych i w stanach zagrażających życiu, można stosować koncentraty czynników krzepnięcia w ciągłym wlewie. Pojawienie się inhibitorów, czyli przeciwciał skierowanych do czynników krzepnięcia jest obecnie najpoważniejszym powikłaniem hemofilii. Jeśli inhibitor pojawi się, to leczenie substytucyjne staje się nieskuteczne. Profilaktyka i leczenie chorych z inhibitorami polega na stosowaniu czynników omijających, których koszty są ogromne, a skuteczność mniejsza niż czynników krzepnięcia u chorych bez inhibitorów. Inhibitor do czynnika VIII pojawia się u około 30% chorych na ciężką postać hemofilii A i u około 3-13% pacjentów z hemofilią A umiarkowaną i łagodną. W hemofilii B inhibitor pojawia się średnio u około 3% chorych. Do powstania inhibitora predysponują: wczesne leczenie dużymi dawkami czynnika krzepnięcia, wylewy i zabiegi operacyjne wymagające intensywnego leczenia substytucyjnego, rodzaj mutacji genu, inhibitor w rodzinie. Do powstania inhibitora najczęściej dochodzi w ciągu pierwszych 50 dni ekspozycji na czynnik krzepnięcia w okresie wczesnego dzieciństwa. W zależności od miana inhibitora chorych dzieli się na 2 grupy: na silnie i słabo reagujących na antygen (high responders i low responders). Jeśli miano inhibitora przekracza 5 jednostek Bethesda, to określa się go jako silny (o wysokim mianie), jeśli miano inhibitora jest zawsze ≤5 jednostek Bethesda, to określany jest jako inhibitor słaby (o niskim mianie). Im wyższe jest miano inhibitora, tym szybciej inaktywowany jest czynnik krzepnięcia. Wystąpienie inhibitora u chorego na ciężką hemofilię nie wpływa na zwiększenie częstotliwości krwawień, ale uniemożliwia skuteczne leczenie i prowadzi do znacznego pogorszenia jakości życia. Inhibitor do czynnika IX wiąże się ze skłonnością do reakcji alergicznych, które występują u około połowy pacjentów i mogą występować pod postacią reakcji anafilaktycznej zagrażającej życiu. Stąd bardzo istotne jest, aby pierwsze podania czynnika IX u chorych były zawsze wykonywane w warunkach szpitalnych. O pojawieniu się inhibitora w umiarkowanej i łagodnej hemofilii mogą świadczyć samoistne wylewy krwi, które z reguły w tych postaciach choroby nie występują. Leczenie chorych z inhibitorem ma dwa cele, czyli trwałą eliminację inhibitora oraz zapobieganie i hamowanie krwawień. Trwałą eliminację inhibitora udaje się osiągnąć u części chorych poprzez wytworzenie stanu immunotolerancji wobec niedoborowego czynnika krzepnięcia. Nie ma jednej skutecznej i niezawodnej metody na przeprowadzenie ITI (wywoływanie tolerancji immunologicznej); każdy ośrodek dobiera leczenie dla swojego pacjenta oparte na doświadczeniach, zależne od zasobów finansowych etc. W Polsce najczęściej stosuje się metodę dużych dawek czynnika krzepnięcia 100-200 j./kg na dobę. Jest to terapia długotrwała, wymagająca dostępu do żył centralnych i bardzo obciążająca, prowadzi się ją nawet do 36 miesięcy. Należy pamiętać, że inhibitor powstaje najczęściej we wczesnym dzieciństwie, a leczenie spoczywa na rodzicach dziecka i odbywa się w warunkach domowych. Szansa na uzyskanie immunotolerancji w ciężkiej hemofilii A wynosi od 70 nawet do 90%. ITI u chorych z hemofilią B jest bardzo problematyczne z uwagi na często występujące ciężkie objawy alergiczne, w tym reakcje anafilaktyczne, które mogą uniemożliwić leczenie pacjenta. Ponadto w hemofilii B w trakcie immunotolerancji często dochodzi do powikłania, jakim jest zespół nerczycowy, który w części przypadków nie ustępuje samoistnie i wymaga przewlekłego leczenia immunosupresyjnego. Leczenie krwawień u chorych z hemofilią powikłaną inhibitorem często stanowi duże wyzwanie. W zależności od sytuacji klinicznej w profilaktyce i leczeniu chorych stosuje się koncentraty czynnika VIII w zwiększonych dawkach, koncentraty aktywowanych czynników zespołu protrombiny (aPCC) i rekombinowany aktywowany czynnik VII (rVIIa), a lekami wspomagającymi są leki antyfibrynolityczne (w Polsce najczęściej stosowany jest kwas traneksamowy). Zabiegi operacyjne u chorych z inhibitorem obarczone są bardzo wysokim ryzykiem krwawienia. Jeśli pacjent bezwzględnie wymaga przeprowadzenia zabiegu, to może być on wykonany w ośrodku referencyjnym, mającym doświadczenie w leczeniu takich chorych. Jeśli u pacjenta nie uda się wywołać immunotolerancji (nieskuteczna ITI), to w Polsce od kilku lat taki pacjent może mieć prowadzoną profilaktykę z zastosowaniem Emicizumabu (przeciwciało monoklonalne zastępujące funkcję czynnika VIII, podawane podskórnie). Jest to leczenie finansowane przez Ministra Zdrowia w ramach modułu „Narodowego Programu Leczenia Hemofilii i Pokrewnych Skaz Krwotocznych na lata 2019-2023” i wymaga uzyskania zgody formalnej, która wydawana jest przez Radę Programu. Do opracowania materiału wykorzystano: Część I: Wytyczne postępowania w hemofilii A i B niepowikłanej inhibitorem czynnika (VIII i IX), wydanie zaktualizowane – 2016 r. (Jerzy Windyga, Krzysztof Chojnowski, Anna Klukowska, Magdalena Łętowska, Andrzej Mital, Jacek Musiał, Jarosław Peregud-Pogorzelski, Maria Podolak-Dawidziak, Jacek Treliński, Anetta Undas, Tomasz Urasiński, Joanna Zdziarska, Krystyna Zawilska) Część II: Wytyczne postępowania w hemofilii A i B niepowikłanej inhibitorem czynnika (VIII i IX), 2 wydanie – 2017 r. (Jerzy Windyga, Krzysztof Chojnowski, Anna Klukowska, Magdalena Łętowska, Andrzej Mital, Wojciech Młynarski, Jacek Musiał, Jarosław Peregud-Pogorzelski, Maria Podolak-Dawidziak, Jacek Treliński, Anetta Undas, Tomasz Urasiński, Joanna Zdziarska, Krystyna Zawilska)

4 października 2023
W leczeniu hemofilii i pokrewnych skaz krwotocznych mają zastosowanie koncentraty czynników krzepnięcia. Przed wprowadzeniem do leczenia koncentratów czynników krzepnięcia duża część chorych umierała przed osiągnięciem wieku dojrzałego. Osocze świeżo mrożone czy krioprecypitat stosowane w leczeniu krwawień wymagały hospitalizacji, miały małą skuteczność i dawały wiele objawów ubocznych, chociażby reakcje alergiczne czy zakażenia wirusami przenoszonymi drogą krwi. Niemożliwe było stosowanie tych preparatów profilaktycznie. Chorzy mieli nawracające krwawienia do stawów, prowadzące do powstania artropatii hemofilowej i w konsekwencji do inwalidztwa, co najczęściej eliminowało ich z życia publicznego i społecznego. Wprowadzenie pierwszych osoczopochodnych koncentratów czynników krzepnięcia ułatwiło znacznie leczenie chorych z hemofilią i umożliwiło stosowanie leczenia domowego, tzw. „leczenia na żądanie” w przypadku krwawień, a w latach kolejnych rozpoczęcie leczenia profilaktycznego, które okazało się niezwykle skuteczne w zapobieganiu krwawieniom. Niestety, jak się później okazało, pierwsze osoczopochodne koncentraty czynników krzepnięcia były przyczyną wystąpienia u znacznej liczby chorych zakażeń wywołanych wirusami HIV, HCV i HBV. Rozwój metod oczyszczania koncentratów czynników krzepnięcia z wirusów przenoszonych drogą krwi umożliwił produkcję bezpiecznych i bardzo skutecznych leków. W większości krajów rozwiniętych standardem leczenia hemofilii jest prowadzenie tzw. leczenia profilaktycznego, które zapobiega występowaniu u chorych samoistnych krwawień do mięśni i stawów oraz krwawień zagrażających życiu. Ten sposób leczenia określany jest też „złotym standardem leczenia hemofilii” i jest rekomendowany dla wszystkich chorych z ciężką postacią hemofilii oraz dla chorych z postacią umiarkowaną, a nawet łagodną z krwotocznym fenotypem. Rozwój metod inżynierii genetycznej umożliwił produkcję koncentratów rekombinowanych czynników krzepnięcia, które powoli zastępują czynniki krzepnięcia osoczopochodne, a są znacznie od nich bezpieczniejsze. Przyszłość leczenia hemofilii to ulepszanie i rozpowszechnianie metod inżynierii genetycznej, co pozwoli na otrzymanie dużych ilości taniego i bezpiecznego czynnika VIII i IX. Koncerny farmaceutyczne opracowują, poddają badaniom klinicznym i wprowadzają na rynek preparaty czynnika VIII i IX o zmodyfikowanej cząsteczce, charakteryzujące się zmniejszoną immunogennością oraz koncentraty czynników krzepnięcia o wydłużonym czasie półtrwania. W latach 1996-2021 w Unii Europejskiej zarejestrowane zostały aż 22 preparaty stosowane w hemofilii. Są to zarówno czynniki krzepnięcia o standardowym czasie półtrwania, o wydłużonym czasie półtrwania, ale też przeciwciało monoklonalne, które zastępuje funkcję czynnika VIII. Zarejestrowane czynniki krzepnięcia VIII i IX poddane pegylacji mogą być stosowane u chorych powyżej 12. roku życia, natomiast czynniki krzepnięcia o wydłużonym czasie półtrwania połączone w drodze fuzji z immunoglobuliną czy albuminą zalecane są dla chorych bez ograniczeń wiekowych. Poniżej znajduje się krótki opis najnowszych, zarejestrowanych w Unii Europejskiej w latach 1996-2021 preparatów, które mogą być stosowane w leczeniu hemofilii i pokrewnych skaz krwotocznych. Eptacog alfa (NovoSeven, producent Novo Nordisk) – to rekombinowany ludzki czynnik krzepnięcia VII aktywowany, wskazany w leczeniu krwawień i zapobieganiu krwawieniom w trakcie zabiegów chirurgicznych lub zabiegów inwazyjnych u pacjentów z wrodzoną hemofilią A i B powikłaną inhibitorem do czynnika krzepnięcia VIII i IX o wysokim mianie; u pacjentów z wrodzoną hemofilią A i B i silną odpowiedzią anamnestyczną na czynnik VIII lub IX; u pacjentów z nabytą hemofilią; u pacjentów z wrodzonym niedoborem czynnika VII; u pacjentów z trombastenią Glanzmanna, u których występuje lub została zgłoszona oporność na przetoczenie płytek krwi lub gdy płytki krwi są niedostępne. Nonacog alfa (BeneFIX, producent Pfizer) – to rekombinowany ludzki czynnik IX, stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii B w każdej grupie wiekowej. Moroctocog alfa (ReFacto AF, producent Pfizer) – to rekombinowany ludzki czynnik krzepnięcia VIII, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A w każdej grupie wiekowej. Octocog alfa (Kogenate, producent Bayer) – to rekombinowany ludzki czynnik krzepnięcia VIII, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A w każdej grupie wiekowej. Catridecacog (NovoThirteen, producent Novo Nordisk) – to rekombinowany ludzki czynnik krzepnięcia XIII; stosowany w długotrwałej profilaktyce i do leczenia krwawień u chorych z wrodzonym niedoborem czynnika XIII we wszystkich grupach wiekowych. Human coagulation factor (Voncento, producent CSL Behring) – to osoczowy ludzki VIII czynnik krzepnięcia i osoczowy ludzki czynnik von Willebranda; stosowany do profilaktyki i leczenia krwawień u pacjentów z chorobą von Willebranda i z hemofilią A we wszystkich grupach wiekowych. Turoctocog alfa (NovoEight, producent Novo Nordisk) – to rekombinowany ludzki czynnik krzepnięcia VIII, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A w każdej grupie wiekowej. Simoctocog alfa (Nuwig, producent Octapharma) – to rekombinowany ludzki czynnik krzepnięcia VIII, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A w każdej grupie wiekowej. Nonacog gamma (Rixubis, producent Takeda) – to rekombinowany ludzki czynnik IX; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii B w każdej grupie wiekowej. Susoctocog alfa (Obizur, producent Takeda) – to rekombinowany wieprzowy czynnik krzepnięcia; stosowany w leczeniu krwawień u chorych z hemofilią A powikłaną inhibitorem do czynnika VIII przeznaczony dla chorych dorosłych. Efmoroctocog alfa (Elocta, producent Swedish Orphan Biovitrum) – to rekombinowany ludzki czynnik krzepnięcia VIII o przedłużonym działaniu, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A w każdej grupie wiekowej. Octocog alfa (Kovaltry, producent Bayer) – to pełnej długości rekombinowany ludzki czynnik krzepnięcia VIII, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A w każdej grupie wiekowej. Albutrepenonacog alfa (Idelvion, producent CSL Behring) – to rekombinowany ludzki czynnik IX o przedłużonym czasie półtrwania; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii B w każdej grupie wiekowej. Eftrenonacog alfa (Alprolix, producent Swedish Orphan Biovitrum) – to rekombinowany ludzki czynnik krzepnięcia IX o przedłużonym działaniu; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii B w każdej grupie wiekowej. Nonacog beta pegol (Refixia, producent Novo Nordisk) – to rekombinowany ludzki czynnik krzepnięcia IX o przedłużonym działaniu; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii B u pacjentów powyżej 12. roku życia. Lonooctocog alfa (Afstyla, producent CSL Behring) – to rekombinowany ludzki czynnik krzepnięcia VIII, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A w każdej grupie wiekowej. Simoctocog alfa (Vihuma, producent Octapharma) – to rekombinowany ludzki czynnik krzepnięcia VIII, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A w każdej grupie wiekowej. Rurioctocog alfa pegol (Adynovi, producent Takeda) – to rekombinowany ludzki czynnik krzepnięcia VIII o przedłużonym działaniu, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A u pacjentów powyżej 12. roku życia. Emicizumab (Hemlibra, producent Roche) – to humanizowane przeciwciało monoklonalne wskazane do stosowania w rutynowej profilaktyce epizodów krwawień u pacjentów z hemofilią A z inhibitorami i bez inhibitorów w każdej grupie wiekowej, jest to jedyny lek do stosowania podskórnego. Voniocog alfa (Veyvondi, producent Takeda) – to rekombinowany ludzki czynnik von Willebranda, zalecany do stosowania u chorych z chorobą von Willebranda do leczenia krwawień chirurgicznych u pacjentów powyżej 18. roku życia. Damactocog alfa pegol (Jivi, producent Bayer) – to rekombinowany ludzki czynnik krzepnięcia VIII o przedłużonym działaniu, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A u pacjentów powyżej 12. roku życia. Turoctocog alfa pegol (Esperoct, producent Novo Nordisk) – to rekombinowany ludzki czynnik krzepnięcia VIII o przedłużonym działaniu, nie zawierający czynnika von Willebranda; stosowany w leczeniu i zapobieganiu krwawieniom w hemofilii A u pacjentów powyżej 12. roku życia. Poniżej zaś znajduje się spis produktów leczniczych, jakie są dopuszczone do obrotu w Polsce do stosowania u pacjentów z hemofilią i pokrewnymi skazami krwotocznymi. Niestety wiele z tych leków jest niedostępnych, a czynniki krzepnięcia o wydłużonym czasie półtrwania są w naszym kraju praktycznie nieosiągalne. Warto jednak znać nazwy czynników krzepnięcia, które otrzymujecie państwo z Regionalnych Centrów Krwiodawstwa i Krwiolecznictwa, ponieważ czasami dystrybuowane są leki o nazwach, które nie są znane ani lekarzom, ani pacjentom. Koncentraty Czynnika VIII: Advate (czynnik VIII rekombinowany o standardowym czasie półtrwania), producent Takeda. Adynovi (czynnik VIII rekombinowany o przedłużonym czasie półtrwania), producent Baxalta/Takeda. Afstyla (czynnik VIII rekombinowany o standardowym czasie półtrwania), producent CSL Behring. Beriate 250 (czynnik VIII osoczopochodny), producent CSL Behring. Elocta (czynnik VIII rekombinowany o przedłużonym czasie półtrwania), producent Swedish Orphan Biovitrum. Emoclot (czynnik VIII osoczopochodny), producent Kedrion. Esperoct (czynnik VIII rekombinowany o przedłużonym czasie półtrwania), producent NovoNordisk. FANHDI (czynnik VIII i czynnik von Willebranda), producent Grifols. Haemate P (czynnik VIII i czynnik von Willebranda), producent CSL Behring. Haemoctin 250 (czynnik VIII osoczopochodny), producent Biotest Pharma GmbH. Immunate 250 IU FVIII/190 IU VWF (czynnik VIII i czynnik von Willebranda), producent Takeda. Innovate 1000j. (czynnik VIII osoczopochodny), producent BIOMED-LUBLIN. Jivi (czynnik VIII rekombinowany o przedłużonym czasie półtrwania), producent Bayer. Kogenate (czynnik VIII rekombinowany o standardowym czasie półtrwania), producent Bayer. Kovaltry (czynnik VIII rekombinowany o standardowym czasie półtrwania), producent Bayer. NovoEight (czynnik VIII rekombinowany o standardowym czasie półtrwania), producent Novo Nordisk. Nuviq (czynnik VIII rekombinowany o standardowym czasie półtrwania), producent Octapharma. Obizur (czynnik VIII rekombinowany wieprzowy), producent Octapharma. Octanate (czynnik VIII osoczopochodny), producent Octapharma. Octanate LV (czynnik VIII osoczopochodny), producent Octapharma. Optivate (czynnik VIII osoczopochodny), producent BPL Bioproducts Laboratory GMBH. Pharmavate (czynnik VIII osoczopochodny), producent Pharma Innovations Sp z o.o. ReFacto (czynnik VIII rekombinowany o standardowym czasie półtrwania), producent Pfizer. Vihuma (czynnik VIII rekombinowany o standardowym czasie półtrwania), producent Octapharma. Voncento (osoczopochodny czynnik VIII i czynnik von Willebranda), producent CSL Behring. Wilate 500 (osoczopochodny czynnik VIII i czynnik von Willebranda), producent Octapharma. Koncentraty Czynnika IX: Alprolix (czynnik IX rekombinowany o przedłużonym czasie półtrwania), producent Swidish Orphan Biovitrum. BeneFix (czynnik IX rekombinowany o standardowym czasie półtrwania), producent Pfizer. Berinin P (czynnik IX osoczopochodny), producent CSL Behring. Betafact (czynnik IX osoczopochodny), producent LBF-Biomedicaments. Idelvion (czynnik IX rekombinowany o wydłużonym czasie póltrwania), producent CSL Behring. Immunine (czynnik IX osoczopochodny), producent Takeda. Octanine (czynnik IX osoczopochodny), producent Octapharma. Refixia (czynnik IX rekombinowany o przedłużonym czasie półtrwania), producent Novo Nordisk. Rixubis (czynnik IX rekombinowany o standardowym czasie półtrwania), producent Takeda. Czynniki omijające: Feiba (koncentrat czynników zespołu protrombiny aktywowany), producent Takeda. NovoSeven (koncentrat aktywowanego rekombinowanego czynnika VII), producent Novo Nordisk. Koncentraty czynnika von Willebranda: Veyvondi (rekombinowany czynnik von Willebranda), producent Takeda. Willafact (osoczopochodny czynnik von Willebranda), producent LBF-Biomedicaments. W Polsce w ramach Narodowego Programu Leczenia Hemofilii i Pokrewnych Skaz Krwotocznych finansowane jest leczenie chorych z zastosowaniem poniżej przedstawionych rodzajów czynników krzepnięcia: koncentrat czynnika VIII, koncentrat rekombinowanego czynnika VIII, koncentrat czynnika IX, koncentrat rekombinowanego czynnika IX, koncentrat czynnika VIII zawierający czynnik von Willebranda w proporcji VWF:FVIII co najmniej 1:1, koncentrat czynnika VIII zawierający czynnik von Willebranda w proporcji VWF:FVIII co najmniej 2:1, koncentrat czynników zespołu protrombiny (PCC), koncentrat aktywowanych czynników zespołu protrombiny (APCC), Emicizumab, koncentrat czynnika VII, koncentrat rekombinowanego czynnika VIIa, koncentrat rekombinowanego wieprzowego czynnika VIII, koncentrat fibrynogenu, koncentrat czynnika XIII, desmopresyna dożylna w ampułkach 4 µg, desmopresyna donosowa. Wybór czynników krzepnięcia stosowanych w leczeniu hemofilii i pokrewnych skaz krwotocznych w Polsce jest na tyle duży, że każdy pacjent chory na skazę krwotoczną powinien mieć zapewnione odpowiednie leczenie w swoim Ośrodku Leczenia Hemofilii. Do opracowania materiału wykorzystano artykuły opublikowane w 2021 roku przez Modern Healthcare Institute „Rozwój terapii w leczeniu skaz krwotocznych-raport”: Rozwój i rejestracje preparatów stosowanych w terapii hemofilii i pokrewnych skaz krwotocznych” – dr n.med. Jakub Gierczyński, MBA

29 września 2023
Organizacja leczenia hemofilii i pokrewnych skaz krwotocznych jest w Polsce bardzo zróżnicowana. Pacjenci z ciężką hemofilią A i B do 18. roku życia objęci są programem lekowym finansowanym przez NFZ. Program lekowy „Zapobieganie krwawieniom u dzieci z hemofilią A i B” wprowadzony został w 2008 roku i od tego czasu każde dziecko z rozpoznaną ciężką postacią hemofilii A i B, za zgodą rodziców, może korzystać z programu od urodzenia do ukończenia 18. roku życia. W programie tym mogą także uczestniczyć pacjenci z hemofilią umiarkowaną, a nawet łagodną, jeśli w przebiegu choroby dochodzi u nich do krwawień dostawowych lub do krwawień zagrażających życiu. Program profilaktyki krwawień u dzieci to kompleksowa opieka nad pacjentem, obejmująca między innymi kontrolne wizyty w Ośrodku Leczenia Hemofilii, dostawy domowe czynnika krzepnięcia, odbiór odpadów medycznych, serwis pielęgniarski, dzienniczki elektroniczne umożliwiające nadzór nad leczeniem pacjenta, czy specjalne aplikacje do monitorowania stężenia czynnika krzepnięcia. Program lekowy dotyczy leczenia profilaktycznego, nie obejmuje leczenia krwawień. Leczenie krwawień i osłona zabiegów chirurgicznych u chorych z hemofilią i innymi skazami krwotocznymi finansowana jest przez Ministerstwo Zdrowia w ramach „Narodowego programu leczenia hemofilii i pokrewnych skaz krwotocznych na lata 2019-2023”. W ramach Narodowego Programu chorzy z hemofilią po 18. roku życia mają możliwość korzystania z profilaktyki krwawień, niektórzy pacjenci objęci są też systemem dostaw domowych. W 2024 roku finansowanie leczenia chorych na hemofilię i pokrewne skazy krwotoczne przejęte zostanie w całości przez NFZ. Wytyczne i zalecenia kliniczne obowiązujące w leczeniu hemofilii na całym świecie zostały zawarte w trzecim wydaniu „Management of Hemofilia” z 2020 roku, opracowanym przez World Federation of Hemofilia. Jest to bardzo obszerny dokument, który wyznacza priorytety opieki oraz opisuje w sposób bardzo dokładny, jak pacjenci chorzy na hemofilię i inne skazy krwotoczne oraz nosicielki hemofilii powinni być diagnozowani i leczeni. Podstawowym priorytetem postępowania w hemofilii A i B jest długoterminowa profilaktyka krwawień. U pacjentów z aktywnością czynnika krzepnięcia poniżej 1% taka forma terapii jest postępowaniem z wyboru i powinna być wdrażana we wczesnym dzieciństwie, natomiast w hemofilii umiarkowanej i łagodnej o konieczności wprowadzenia profilaktyki decyduje przebieg kliniczny choroby, czyli liczba i rodzaj krwawień. Wraz z rozwojem nowych technologii i pojawianiem się nowych leków definicja profilaktyki krwawień hemofilii uległa ewolucji. Pojawienie się, obok osoczopochodnych, rekombinowanych czynników krzepnięcia, a także czynników krzepnięcia o wydłużonym czasie półtrwania i pierwszej terapii niesubstytucyjnej zmieniło na świecie podejście do leczenia profilaktycznego, poprawiło jego skuteczność oraz umożliwiło efektywniejsze leczenie tych chorych, u których standardowa profilaktyka była nieskuteczna lub częściowo skuteczna. Początkowo uważano, że leczenie profilaktyczne powinno zabezpieczyć pacjenta przed krwawieniami samoistnymi, a aktywność czynnika VIII lub IX nie powinna spadać poniżej 1%. Stosowane były schematy profilaktyczne polegające na podawaniu standardowych stałych dawek czynników krzepnięcia 2 lub 3 razy w tygodniu. I rzeczywiście pacjenci z reguły nie mieli krwawień zagrażających życiu, ale zdarzały się krwawienia samoistne i pourazowe oraz mikrokrwawienia, które mogły doprowadzić do uszkodzeń stawów i w efekcie do artropatii hemofilowej. Tak prowadzona profilaktyka nie dla każdego pacjenta była skuteczna. Nowe terapie i spersonalizowanie profilaktyki, czyli dostosowanie profilaktyki do indywidualnych potrzeb pacjenta mają doprowadzić do całkowitego wyeliminowania krwawień samoistnych i zgodnie z wytycznymi zawartymi w dokumencie WFH zapewnić chorym jakość życia porównywalną z ich zdrowymi rówieśnikami. Jest to możliwe do osiągnięcia u większości chorych na hemofilię, w tym wszystkich dzieci, pod warunkiem dostępności nowoczesnych terapii. Indywidualizacja leczenia chorych na hemofilię polega na odpowiednim dobraniu dawek czynnika krzepnięcia na podstawie uzyskanych wyników badań farmakokinetycznych dla stosowanego leku zależnie od indywidualnych potrzeb pacjenta. Każdy chory jest inny, każdy ma inny czas półtrwania czynnika krzepnięcia i każdy potrzebuje innego leczenia. Pacjenci z uszkodzonymi stawami wymagają wyższych dawek czynnika krzepnięcia i częstszego podawania, aby nie dopuścić do tzw. „krwawień przebijających”. Chorzy aktywni zawodowo, pracujący fizycznie, uprawiający intensywnie sport potrzebują innego leczenia niż chorzy pozostający w domu, dla których aktywność fizyczna ogranicza się do przysłowiowego „oglądania telewizora”. Aby pacjent z hemofilią mógł mieć zastosowaną zindywidualizowaną terapię, czyli terapię najbardziej optymalną dla siebie, konieczna jest ścisła współpraca pomiędzy pacjentem i lekarzem Ośrodka Leczenia Hemofilii oraz dostęp do specjalistycznego laboratorium. U pacjenta konieczne jest wykonanie badań farmakokinetycznych, które polegają na pobieraniu i oznaczaniu aktywności czynnika krzepnięcia we krwi w różnych punktach czasowych po podaniu ostatniej dawki leku. Dla lekarzy w Ośrodkach Leczenia Hemofilii dostępne są aplikacje, które umożliwiają bardzo dokładne wykonanie farmakokinetyki dla różnych czynników krzepnięcia, a także ustalenie właściwych dawek leków dla pacjenta, w zależności od indywidualnych potrzeb. Program lekowy stosowany u dzieci od 2020 roku pozwala na personalizowaną profilaktykę czynnikiem krzepnięcia VIII, zgodną z zapisami w karcie Charakterystyki Produktu Leczniczego (ChPL). Niektóre dzieci mają bardzo krótki czas półtrwania czynnika krzepnięcia, a zgodnie z ChPL nie mogą otrzymać wyższej dawki leku i właśnie u nich pełna personalizacja nie jest możliwa. Dużym ograniczeniem jest też dostęp do żył obwodowych w przypadku konieczności podawania czynnika krzepnięcia co drugi dzień lub w wyjątkowych przypadkach nawet codziennie. U dorosłych nie obowiązuje tak sztywny schemat terapii, nie ma ograniczeń dotyczących dawki czy częstości podania leku. Schemat leczenia u osób dorosłych można dostosować do obrazu klinicznego choroby i potrzeb pacjenta, co jest postępowaniem optymalnym i stwarzającym największe szanse na pełną eliminację krwawień, ale wymaga ścisłej współpracy pacjenta z lekarzem. W Polsce dla osób dorosłych dostępne są od wielu lat osoczopochodne czynniki krzepnięcia, sporadycznie czynniki rekombinowane, co wynika z procedur przetargowych. W przypadku uczulenia na osoczowe czynniki krzepnięcia możliwe jest leczenie czynnikami rekombinowanymi. Konieczne jest jednak zgłoszenie takiego pacjenta przez lekarza do Narodowego Centrum Krwi i uzyskanie zgody na inną terapię. Indywidualizacja leczenia dotyczy także jakości życia chorych, która wiąże się z częstotliwością wykonywania iniekcji i czasem potrzebnym do podania leku. Brak w Polsce dostępności do czynników o przedłużonym czasie półtrwania dla pacjentów, którzy, dążąc do całkowitego wyeliminowania krwawień, potrzebują bardzo częstego podawania leku, stanowi problem w leczeniu hemofilii. Uciążliwość związana z dożylnym podawaniem leku powoduje, że część pacjentów świadomie zmniejsza jego częstość, akceptując ryzyko i pewną liczbę krwawień za cenę rzadszego wykonywania iniekcji. Część pacjentów nie akceptuje konieczności ciągłego stosowania profilaktyki. Niestety dotyczy to także dzieci, których rodzice nie potrafią lub nie są w stanie zapewnić dzieciom regularnych podań leku. W wielu przypadkach problemem jest brak odpowiedniej świadomości potrzeb chorego dziecka i w konsekwencji nieprzestrzeganie zasad terapii. W przypadku osób dorosłych to decyzje świadome, a w przypadku młodych dorosłych i młodocianych pacjentów forma buntu lub sprawdzenia, jak to jest bez profilaktyki. Podstawą leczenia hemofilii jest leczenie domowe. Umożliwia to stosowanie profilaktycznych podań czynnika krzepnięcia, a także szybkie podanie leku w przypadku wystąpienia krwawienia. Wszyscy pacjenci w Polsce chorzy na hemofilię mają możliwość posiadania w domu czynnika krzepnięcia i dostępu do niego w każdym momencie. W Ośrodkach Leczenia Hemofilii prowadzona jest edukacja rodziców i dzieci w celu nabycia umiejętności wykonywania iniekcji zarówno przez rodziców, jak również przez starsze dzieci, co umożliwia właściwe prowadzenie leczenia. W ramach programu lekowego dostępne są także pielęgniarki-edukatorki, które prowadzą szkolenia w warunkach domowych. Ośrodki Leczenia Hemofilii dysponujące wyspecjalizowaną kadrą powinny znajdować się przy każdej klinice hematologii. W praktyce wygląda to mniej optymistycznie, głównie z powodu braku specjalistów z odpowiednią wiedzą z zakresu zaburzeń hemostazy. O ile pacjenci z hemofilią raczej nie mają kłopotów z zaopatrzeniem się w czynniki krzepnięcia do profilaktyki i leczenia w warunkach domowych, to w przypadku pojawienia się konieczności przeprowadzenia poważnego zabiegu operacyjnego mogą pojawić się poważne problemy w znalezieniu odpowiedniego ośrodka, w którym taki zabieg można wykonać. Leczenie chorych na hemofilię w Polsce znacznie poprawiło się w ciągu ostatnich 20 lat. Zmniejszyła się znacznie liczba zgonów chorych w młodym wieku i ograniczona została liczba przypadków inwalidztwa narządu ruchu dzięki wprowadzeniu skutecznego leczenia profilaktycznego. Właściwa profilaktyka umożliwia młodym chorym z hemofilią prowadzenie życia identycznego, jak ich zdrowi rówieśnicy. Mogą uczestniczyć w życiu społecznym i podejmować aktywności związane z nauką i pracą. Poziom leczenia hemofilii jest bardzo wysoki, ale poprzeczkę zawsze można podnieść wyżej. Życie bez krwawień w hemofilii jest możliwe, chociaż aby osiągnąć cel „zero bleeds” potrzebne jest ogromne zaangażowanie samego chorego, lekarza i całego środowiska. Pacjenci dorośli, którzy mają zmiany w stawach, wymagają bezwzględnie prowadzenia profilaktyki tzw. wtórnej krótko- lub długoterminowej, dostępu do specjalistów ortopedów i przede wszystkim do rehabilitacji. Hemofilia jest jedną z wielu skaz krwotocznych, której leczenie jest finansowane w ramach Narodowego Programu Leczenia Hemofilii i Pokrewnych Skaz Krwotocznych. Każda skaza krwotoczna stanowi odmienną jednostkę chorobową, która może mieć kilka postaci i typów. Wielu skaz krwotocznych nie leczy się profilaktycznie, a jedynie wtedy, gdy dojdzie do krwawienia lub konieczny jest zabieg chirurgiczny. Leczenie niektórych skaz krwotocznych jest bardzo złożone i niezwykle kosztowne, chociażby nabyta hemofilia A czy nabyty zespół von Willebranda. Różne skazy krwotoczne wymagają stosowania różnych leków, a nie zawsze są dostępne czynniki krzepnięcia, które mogą być stosowane do leczenia krwawień. Pozostaje wówczas stosowanie leków najstarszych, czyli osocza świeżo mrożonego lub krioprecypitatu. Aby leczenie skaz krwotocznych w Polsce można było podnieść na wyższy poziom, konieczne jest stworzenie sieci sprawnie działających, kompleksowych ośrodków, które byłyby obecne w każdym mieście wojewódzkim, połączonych ze sobą odpowiednim systemem informatycznym, tworzącym bazę danych i pozwalającym na prowadzenie rejestru medycznego. Wymaga to wieloletnich działań i wprowadzenia zmian systemowych, w tym również zwiększenia nakładów finansowych na rozwój poszczególnych obszarów związanych z opieką nad chorym ze skazą krwotoczną. Do opracowania materiału wykorzystano artykuły opublikowane w 2021 roku przez Modern Healthcare Institute „Rozwój terapii w leczeniu skaz krwotocznych-raport”: „Praktyka kliniczna leczenia hemofilii w Polsce” – dr n. med. Joanna Zdziarska, Krzysztof Jakubiak

3 lipca 2023
Planowanie podróży i wakacji za granicą – lista zadań Jeśli w planach są wakacje zagraniczne, trzeba być dobrze zorganizowanym i mieć pewność, że wszystko znajduje się na swoim miejscu. Odpowiednio wcześnie rozpocząć planowania we współpracy z lekarzem kierującym, by upewnić się co do wystarczającej ilość czynnika krzepnięcia, sprzętu, innych leków, listów od lekarza. Upewnić się co do posiadania niezbędnych dokumentów medycznych, celnych i dotyczących kwarantanny dla produktu leczniczego i sprzętu zarówno na wyjazd i na powrót do kraju, jak i na wjazd i powrót z państwa, które odwiedzacie. Pamiętać, że nawet podczas podróży tranzytowych przez kraj mogą istnieć wymagania dotyczące dokumentacji w związku z przewozem czynnika krzepnięcia, igieł, innych leków przez kontrolę bezpieczeństwa/kwarantanną/odprawą celną na lotniskach. Starannie wybierać miejsce, cel podróży, zwłaszcza jeśli pojawi się potrzeba pomocy medycznej. Należy sprawdzić, czy w odwiedzanych miejscach istnieje specjalistyczna opieka i funkcjonuje leczenie osób ze skazą krwotoczną oraz w jaki sposób można uzyskać dostęp do takich usług. Leczenie może być ograniczone, niedostępne lub zbyt drogie w wielu krajach. Należy się upewnić co do odpowiedniego ubezpieczenia podróżnego i planu na wypadek krwawienia lub wypadku. Należy skontaktować się z hotelem, aby dowiedzieć się, czy jest tam dostęp do lodówki, co umożliwi przechowywanie leków w niskiej temperaturze. W przypadku dodatkowych zapasów czynnika krzepnięcia na podróż, należy zadbać o nie podczas podróży i zabrać ze sobą resztki produktu z powrotem. Lista kontrolna na podróż zagraniczną Pamiętaj, aby: Być przygotowanym i planować Porozmawiać z ośrodkiem leczenia hemofilii z odpowiednim wyprzedzeniem, aby na czas zorganizować produkty lecznicze, dokumentację itp. Wykupić ubezpieczenie turystyczne Wspomnieć o skazie krwotocznej, jeśli w kwestionariuszu do ubezpieczenia podróżnego pojawia się pytanie o „istniejące wcześniej schorzenia”, aby uniknąć problemów z ubezpieczeniem w razie wystąpienia problemów podczas podróży Poinformować osoby, z którymi się podróżuje, o skazie krwotocznej i o tym, co zrobić, jeśli potrzebna jest pomoc. Nigdy nie wiadomo, kiedy i gdzie może się taka sytuacja wydarzyć Upewnić się, że masz ze sobą odpowiednią dokumentację na temat diagnozy, zalecanego leczenia, osób, z którymi należy się kontaktować w nagłych wypadkach Wybrać takie torby bagażowe, które nie będą negatywnie wpływać na mięśnie pleców, ramion czy karku, na przykład torba na kółkach. Jeśli nosisz torbę na jedno ramię, pamiętaj o częstym zmienianiu strony, by uniknąć nadwyrężenia jednej strony pleców lub ramienia. Pomocna może się okazać np. konsultacja z fizjoterapeutą dla uzyskania indywidualnych wskazówek na temat bezpiecznego przewożenia bagażu Zrobić kserokopię dokumentów podróżnych (paszportu, planu podróży, ubezpieczenia podróżnego, listów od lekarzy) i zostawić je np. w domu Zaopatrzyć się w odpowiednią dokumentację potrzebną do odprawy celnej i kontroli bezpieczeństwa. Skontaktuj się w tej sprawie z ośrodkiem leczenia hemofilii na co najmniej 3 miesiące przed podróżą, by mieć odpowiednią ilość czasu na ich zebranie. Pamiętaj, że podczas kontroli może zajść potrzeba zbadania okładów z lodu, ponieważ mogą zostać uznane za przekraczające limit płynów możliwych do wniesienia na teren samolotu, dlatego taka dokumentacja jest konieczna! Poinformować lekarza prowadzącego dokładnie, dokąd się udajesz, ponieważ w niektórych państwach konieczne jest zatwierdzenie wywozu lub wwozu produktów leczniczych Rozważyć przetłumaczenie dokumentacji na język kraju, do którego się udajesz Być cierpliwym podczas kontroli granicznej. Nie zakładaj, że urzędnicy celni mają wiedzę na temat skaz krwotocznych! Zabrać ze sobą produkt leczniczy, jeśli potrzebujesz regularnego leczenia na żądanie Zaopatrzyć się w wystarczającą ilość leków, by zapewnić sobie rezerwę na 24-48 godzin, by dostać się do kraju, w którym można uzyskać dostęp do odpowiedniej opieki medycznej. W przypadku okresu profilaktyki, należy zabrać ze sobą wszystkie leki wymagane na dłuższe podróże lub zorganizować dostawę większej ilości za granicę Pamiętać, że Twój produkt leczniczy może nie być dostępny w kraju, do którego podróżujesz, a uda Ci się dotrzeć jedynie do produktów pochodzących z osocza o innym zakresie, rekombinowanych i niezawierających czynnika Ze względu na różny stan materialny poszczególnych państw, zaopatrzyć się we własny sprzęt do leczenia i iniekcji Pamiętać, że może pojawić się konieczność opłacenia potrzebnego Ci produktu leczniczego, co ma szansę być bardzo kosztowne, dlatego tak ważne jest ubezpieczenie podróżne! Pamiętać, że niewykorzystanych produktów leczniczych nie można zwrócić! Źródła: https://www.haemophilia.org.au/ https://www.factoredin.org.au/ https://stepsforliving.hemophilia.org/first-step/family-life

30 czerwca 2023
Przedstawiamy Państwu broszurę pt. "Hemofilia w pigułce dla personelu medycznego", w której zawarte są najważniejsze informacje dotyczące profilaktyki, diagnozy, leczenia oraz powikłań hemofilii. https://issuu.com/hematoonkologia.pl/docs/takedamed-hemofilia-w-pigulce?fr=sZjIyZjE5NDUzNTM

26 czerwca 2023
Przedstawiamy Państwu broszurę pt. "Opieka nad „Portem” w domu Pacjenta", w której zawarta jest instrukcja, jak zadbać o port osoby chorej. https://issuu.com/hematoonkologia.pl/docs/takedamed-opieka-nad-portem?fr=sZTg4YjE5NDUzNTM

Diagnoza hemofilii ma ogromny wpływ na całe życie zarówno osoby chorej, jak i całej jej rodziny. Związana jest z nieustannym planowaniem i ochroną przez jakimikolwiek urazami. Dlatego też wiele osób z taką diagnozą uznaje, że w ich sytuacji dalekie podróże i poznawanie świata jest niemożliwe. W tym artykule chcemy jednak pokazać, że z hemofilią można, a nawet warto wyjeżdżać, zarówno z całą rodziną, jak i samodzielnie. Potrzebne jest jednak odpowiedni sposób przygotowania, zaopatrzenie i dokumentacja, o czym znajdziecie więcej informacji poniżej. Czy osoby z hemofilią mogą podróżować? Tak! Wymaga to jednak większego zaangażowania przy organizacji oraz przygotowaniu bagaży. Konieczny będzie przede wszystkim kontakt z lekarzem prowadzącym w celu zorganizowania wystarczającej ilości produktów leczniczych i sprzętu na czas nieobecności. Osoby chore lub ich opiekunowie muszą dowiedzieć się, gdzie znajdują się ośrodki leczenia hemofilii najbliższe miejsca ich pobytu. Mogą także potrzebować dokumentacji, by przewieźć leki i sprzęt do leczenia przez kontrolę bezpieczeństwa oraz odprawę celną. Bardzo ważne jest, by porozmawiać na ten temat ze specjalistami z odpowiednim wyprzedzeniem, pamiętając o rezerwacji czasu na przygotowanie dokumentacji. List podróżny Kiedy planujecie wyjazd, konieczne jest przede wszystkim zaopatrzenie się w recepty na czynnik krzepnięcia. Pomocą może okazać się także list, gdzie znajduje się opis stanu osoby z hemofilią oraz zasady podawania leków. Wzór dokumentu Co musimy zrobić, jeśli chcemy wyjechać? Każdy ma indywidualne potrzeby związane z podróżą, dlatego warto skontaktować się z lekarzem prowadzącym na kilka miesięcy przed wyjazdem, by podróż zaplanować z wyprzedzeniem. Szczególnie istotna pomoc może się przydać w organizacji podróży zagranicznej, przystosowana w zależności od indywidualnej sytuacji. Specjaliści powinni umieć doradzić w sprawie koniecznej dokumentacji, leków, ubezpieczenia podróżnego. Na wszelki wypadek warto odszukać dane kontaktowe Ośrodków Leczenia Hemofilii, które znajdują się na trasie podróży. Warto zastanowić się również, czy dobrze by było poinformować osoby współtowarzyszące, co mają robić w razie niebezpieczeństwa. Jeśli podróż odbywa się samolotem, należy poprosić lekarza kierującego o przygotowanie listu potwierdzającego, że czynnik oraz igły i strzykawki muszą być przewożone na pokładzie, w części kabinowej, ponieważ przebywając w luku bagażowym w samolocie, produkty te narażone są na ekstremalne temperatury, co może mieć na nie negatywny wpływ. W przypadku, gdy podróżuje dziecko z hemofilią, który ma wszczepialny port naczyniowy, należy poprosić o list potwierdzający, że w bagażu podręcznym muszą znajdować się takie materiały eksploatacyjne, jak „czynnik”, „igły do obsługi portu”, „środki dezynfekcyjne”, „port naczyniowy”. O obecności tego typu urządzeń należy poinformować wcześniej osoby przeprowadzające kontrolę, warto wspomnieć wtedy o posiadaniu listu lekarskiego. Okazanie takiego listu może nie być konieczne, ale lepiej się na taką sytuację przygotować. Czynnik może bez szkody przejść przez skaner podczas kontroli bezpieczeństwa na lotnisku Pamiętaj także, że ochrona lotnicza ma również ograniczenia dotyczące zasad przenoszenia płynów, aerozoli i żeli. Produkty i urządzenia medyczne są zwolnione z tych ograniczeń, ale musisz mieć ze sobą odpowiednią dokumentację. Ile Należy pamiętać, że żele lub okłady z lodu nie są zwolnione z tych zasad i możesz nie być w stanie przenieść ich przez kontrolę bezpieczeństwa. Bardzo istotne jest więc, by mieć przy sobie listy opisujące produkt, aktywne składniki, jego prezentację i liczbę fiolek, które przenosicie. Listy muszą stwierdzać, że produkt jest przeznaczony do użytku osobistego i że fiolek nie wolno otwierać podczas kontroli. Produkt należy przewozić w oryginalnym opakowaniu. Oznacza to, że nie należy rozpakowywać fiolek z opakowania w celu zaoszczędzenia miejsca. Może zaistnieć potrzeba zgłoszenia produktu w niektórych punktach kontroli bezpieczeństwa i urzędach celnych, dlatego w razie potrzeby koniecznie przechowujcie listy w łatwo dostępnym miejscu. Podczas wszystkich podróży należy nosić produkt w torbie izolacyjnej. Mimo że większość produktów można przechowywać w temperaturze pokojowej, bardzo łatwo je przegrzać podczas upałów, szczególnie w samochodach czy na kempingu. Należy rozważyć zabranie ze sobą apteczki pierwszej pomocy. Oto kilka produktów, które mogą okazać się przydatne: Zimne okłady typu „suchy lód” lub worek na okłady z lodu; Medyczny spray chłodzący; Szalik, który można wykorzystać jako temblak; Środek przeciwbólowy – paracetamol; Sztyft ściągający do małych skaleczeń i otarć; Spray do nosa; Tabletki z kwasem traneksamowym na krwawienia z jamy ustnej i nosa. Przydatne może się także okazać pamiętanie o metodzie RICE (Rest, Ice, Compress, Elevate). Po powrocie pamiętajcie, żeby od razu upewnić się czy wykorzystane zostały wszystkie produkty lecznicze. Choć podróżowanie z hemofilią jest ogromnym wyzwaniem organizacyjnym, zachęcamy, by mimo wszystko próbować się go podjąć i zapewnić sobie i swoim najbliższym wspaniały i niezapomniany czas wypoczynku. Szerokiej drogi! Źródła: https://www.haemophilia.org.au/ https://www.factoredin.org.au/ https://stepsforliving.hemophilia.org/first-step/family-life

19 czerwca 2023
Aktywność fizyczna stanowi ważną część zdrowego trybu życia. Udział w sportach, grach oraz wykonywanie ćwiczeń to powiązany z zabawą sposób na poprawę jakości Twojego życia – zarówno fizycznego, umysłowego, jak i emocjonalnego. Fakt, że masz hemofilię, tego nie zmienia. Aktywność fizyczna pomoże Ci rozwinąć mocne kości i silne mięśnie chroniące stawy przed urazami, dlatego jej znaczenie w Twoim wypadku może być o wiele większe. Sport pomaga również w utrzymaniu pozytywnego nastawienia oraz spojrzenia na życie. Nie musisz czuć żadnych ograniczeń. W tej broszurze przedstawiamy korzyści oraz zagrożenia, jakie niosą ze sobą wybrane dyscypliny sportu. Ważne jest jednak, abyś swoje plany omówił z lekarzem lub innym wykwalifikowanym pracownikiem medycznym, znającym Twoją sytuację. Tylko taka osoba może udzielić właściwych rad oraz dobrać odpowiedni zestaw ćwiczeń. https://issuu.com/hematoonkologia.pl/docs/takedamed-hematologia-cwiczenia?fr=sZGJjMjE5NDUzNTM

16 czerwca 2023
Przedstawiamy Państwu broszurę pt. "Hemofilia kobiecym okiem", w której zawarte są najważniejsze informacje, jakie każda nosicielka hemofilii powinna wiedzieć. Z materiału między innymi dowiemy się, co to hemofilia, skąd się bierze, jakie są jej objawy oraz jak się ją leczy. https://issuu.com/hematoonkologia.pl/docs/takedamed-hemofilia-kobiecym-okiem?fr=sYTY2NjE5NDUzNTM

5 czerwca 2023
Jednym z podstawowych działań wzmacniających nasze zdrowie jest właściwe odżywianie. Dieta jest prostym, a do tego bezpiecznym sposobem zachowania zdrowia i dbania o nie. Dobrze jest mieć świadomość, że poprzez odpowiedni dobór składników spożywczych i poprzez świadome gotowanie możemy wspierać proces zdrowienia. Wchodząc do kuchni i biorąc się za przygotowywanie posiłków, bierzemy odpowiedzialność za własne zdrowie. https://issuu.com/hematoonkologia.pl/docs/takedamed-jak-wzmocnic-zyly?fr=sZGVhZTE5NDUzNTM

31 maja 2023
Hemofilia to choroba występująca sporadycznie. Jej rzadkość jest jednym z powodów istnienia różnychmitów i błędnych przekonań na jej temat. Często są one powodem tego, że życie osób z hemofilią lub osób z ich otoczenia jest o wiele bardziej skomplikowane. Przedstawiamy Państwu broszurę, którą możecie przekazać nauczycielom i opiekunom Waszych dzieci. Ta broszura ma za zadanie dostarczyć nauczycielom oraz ich uczniom informacji koniecznych do zagwarantowania, że dziecko z hemofilią lub innym wrodzonym zaburzeniem krzepnięcia krwi dobrze czuje się w szkole i korzysta z niej w takim samym stopniu, jak inne dzieci. https://issuu.com/hematoonkologia.pl/docs/takedamed-hemofilia-w-klasie_11d99818cb1c20?fr=sOTYwMzE5NDUzNTM

14 kwietnia 2023
Serdecznie zapraszamy na warsztaty edukacyjne z okazji Światowego Dnia Chorych na Hemofilię, które odbędą się w formie hybrydowej 16.04.2023 r. Podczas spotkania wysłuchamy wykładów ekspertów dotyczących organizacji ośrodka leczenia hemofilii oraz pracy koordynatorek, dowiemy się na jakich zasadach chory otrzymuje dostawy domowe czynnika, jak prawidłowo obsługiwać port dożylny oraz jak zadbać o swoje zdrowie, które zaczyna się w głowie. Oficjalna strona wydarzenia

13 lutego 2023
Hemofilia nie jest bezpośrednim wskazaniem do rezygnacji z posiadania potomstwa. Większość nosicielek hemofilii przeżywa ciążę bez komplikacji i krwawień. Jak przejść przez ten czas, aby uniknąć niebezpiecznych sytuacji? Oto kilka porad dla przyszłej mamy z hemofilią. Pamiętaj, że ten artykuł ma jedynie funkcję informacyjną i nie zastępuje konsultacji lekarskich. Wszelkie szczegółowe informacje przekaże Ci Twój lekarz hematolog oraz ginekolog prowadzący ciążę. Zadbaj o kompleksową opiekę medyczną Nie tylko ginekolog i położna – ale także Twój lekarz hematolog powinien czuwać nad przebiegiem ciąży. Zapytaj o specjalistę ginekologa w lokalnym ośrodku leczenia hemofilii. Dzięki jego doświadczeniu w prowadzeniu ciąży kobiet ze skazami krwotocznymi będzie w stanie zapewnić Ci prawidłową opiekę i zwróci uwagę na kwestie, których „zwykły” ginekolog może nie zauważyć. Listę ośrodków realizujących „Narodowy Program Leczenia Chorych na Hemofilię i Pokrewne Skazy Krwotoczne na lata 2019-2023” znajdziesz pod tym linkiem: www.gov.pl/web/nck/lista-osrodkow-realizujacych-narodowy-program-leczenia-chorych-na-hemofilie-i-pokrewne-skazy-krwotoczne-na-lata-2019-2023 Wszelkie wątpliwości i pytania kieruj do swojego lekarza Nie szukaj informacji na własną rękę. Nie bój się pytać – obowiązkiem lekarza prowadzącego jest informowanie Ciebie jako jego pacjentki o wszelkich aspektach stanu zdrowia – Twojego i Twojego dziecka. Zbieraj dokumentację medyczną w jednym miejscu Wyniki badań, zalecenia lekarskie, listę przyjmowanych leków uporządkuj w jednym miejscu, aby dawały lekarzom jasny obraz Twojego stanu zdrowia. Poznaj historię swojej rodziny Na ile to możliwe, spróbuj uzyskać szczegółowe informacje o przypadkach hemofilii w Twojej rodzinie (jeśli takie występują). Są to informacje przydatne dla zespołu lekarskiego, umożliwiające lepsze ustalenie genetycznych uwarunkowań Twojej hemofilii. Unikaj inwazyjnych zabiegów Na co dzień pamiętasz o tym, aby ostrożnie podchodzić np. do zabiegów dentystycznych. W ciąży Twoja ostrożność powinna się podwoić – najlepiej, jeśli na ten czas zupełnie zrezygnujesz z zabiegów mogących spowodować u Ciebie krwawienie (chyba, że będą one konieczne dla Twojego zdrowia czy życia). Wszystkie decyzje w tej materii konsultuj z lekarzem. Wykonaj badania prenatalne Jednym z podstawowych badań prenatalnych jest określenie płci dziecka, wykonywane zazwyczaj po 16 tygodniu ciąży. Określenie płci jest w tym przypadku istotne ze względów medycznych. Jeśli dziecko to chłopiec, prawdopodobieństwo, że będzie miało hemofilię jest wyższe niż w przypadku dziewczynki. W tej sytuacji zespół medyczny może przeprowadzić dalsze, bardziej inwazyjne badania – amniopunkcję lub pobranie kosmówki (niosą one za sobą pewne ryzyko dla zdrowia dziecka i przebiegu ciąży, ich wykonanie należy więc przedyskutować z zespołem lekarskim). Gdy u chłopca potwierdzona zostanie skaza krwotoczna, wówczas procedury około- i poporodowe zostaną przeprowadzone według odpowiednich wymogów bezpieczeństwa. To także znak dla Ciebie (i partnera) – aby rozpocząć przygotowania do opieki nad noworodkiem z hemofilią. Planuj z wyprzedzeniem Zapisuj ważne daty – np. poszczególnych wizyt u lekarza czy badań laboratoryjnych. To ważne, abyś porządkowała obowiązki związane z byciem mamą już na etapie ciąży. Może się to wydawać rygorystyczne, wiadomo też, że życie bywa nieprzewidywalne – ale będziesz się czuła bezpieczniej, kiedy utrzymasz kontrolę nad małymi codziennymi wyzwaniami. Prawidłowo się odżywiaj To porada, którą przekazuje się każdej kobiecie ciężarnej. Zdrowa i zbalansowana dieta w ciąży jest bardzo istotna dla prawidłowego rozwoju dziecka oraz Twojego samopoczucia. Poszukaj wsparcia psychologicznego Nie jesteś sama. Możesz odczuwać strach i zagubienie; dla wielu kobiet czas ciąży (szczególnie w pierwszym trymestrze) wiąże się ze zmiennością nastrojów czy przygnębieniem. To naturalne dla każdej mamy – gospodarka hormonalna kobiety ciężarnej przechodzi gwałtowne zmiany, co wpływa na jej ciało i umysł. W związku z nosicielstwem hemofilii możesz odczuwać swego rodzaju poczucie winy – że możesz „obarczyć” swoje dziecko skazą krwotoczną. To pułapka, z której trzeba wyjść jak najszybciej. Podarujesz swojemu dziecku największy dar – dar życia i to się w tej sytuacji liczy. Choć ciąża i macierzyństwo, szczególnie w obliczu skazy krwotocznej, jest wyzwaniem, może być także pięknym doświadczeniem. Zapytaj w ośrodku leczenia hemofilii o możliwość skorzystania z pomocy psychologa/psychoterapeuty. Poszukaj informacji o pacjenckich organizacjach czy grupach wsparcia dla mam, w których możesz spotkać kobiety w podobnej sytuacji bądź bardziej doświadczone, służące radą. Grupa Hemofilia Polska: www.facebook.com/groups/1699726933599700 Polskie Stowarzyszenie Chorych na Hemofilię www.hemofilia.org.pl Stowarzyszenie Chorych na Wrodzone Skazy Krwotoczne www.scwsk.org.pl Dowiedz się jak najwięcej jeszcze przed zajściem w ciążę W przypadku nosicielstwa hemofilii, dobrze jest zasięgnąć porady lekarza hematologa i dowiedzieć się o przebiegu ciąży i porodu u kobiet ze skazą krwotoczną jeszcze w momencie planowania powiększenia rodziny. Istotna jest także rozmowa z partnerem na temat rodzicielstwa i wyzwań związanych z hemofilią u Ciebie jako matki oraz (potencjalnie) dziecka. Czy wiesz, że… Poziomy czynnika VIII znacznie wzrastają w czasie ciąży, co zmniejsza ryzyko krwawienia u nosicielek hemofilii A. Inaczej jest z poziomem czynnika IX – on w czasie ciąży nie rośnie. Poziomy czynników powinny być badane w trzecim trymestrze ciąży wtedy, gdy są najwyższe. Jeśli nie są wystarczająco wysokie, lekarze podejmują środki ostrożności, aby zmniejszyć ryzyko nadmiernego krwawienia podczas porodu. Kilka słów o porodzie Nie da się ukryć – poród u nosicielki hemofilii jest wydarzeniem bardziej wymagającym niż u kobiety bez skazy krwotocznej. Dzięki odpowiednim przygotowaniom, wiedzy i umiejętnościom personelu medycznego, może on jednak przebiec bezpiecznie i bez większych powikłań. Brak jest danych klinicznych na temat ryzyka powikłań poporodowych u nosicielek hemofilii w przypadku porodu naturalnego i cięcia cesarskiego. Przyjmuje się, że – jeśli to możliwe – należy dołożyć starań, aby poród nastąpił drogą naturalną. Poród powinien odbywać się w ośrodku współpracującym z laboratorium wykonującym oznaczenia aktywności czynników krzepnięcia. Ważne jest także zabezpieczenie krwi do ewentualnej transfuzji. Według wytycznych dla ginekologów-położników koncentrat niedoborowego czynnika krzepnięcia podaje się rodzącej natychmiast po rozpoczęciu akcji porodowej, a w przypadku cięcia cesarskiego – przed rozpoczęciem zabiegu. Matki będące nosicielkami genu hemofilii są narażone na poważne krwawienie także po porodzie. Dzieje się tak dlatego, że wysoki poziom czynnika VIII podczas ciąży spada do niższego poziomu po porodzie. Dłuższe krwawienie z kanału rodnego, tzw. krwotok poporodowy, może wymagać leczenia w celu zatrzymania krwawienia. Jeśli wiadomo, że dziecko także ma hemofilię, lekarze z dużą ostrożnością przyjmują poród i unikają używania narzędzi takich jak kleszcze. Zdarza się, że dziecko krwawi, np. z uszkodzonej skóry na głowie lub po nakłuciu żyły podczas pobierania krwi do badań, takie krwawienia zazwyczaj nie wymagają leczenia i nie dają żadnych powikłań. Jeśli w trakcie porodu dojdzie do krwawienia do centralnego układu nerwowego wówczas konieczne jest intensywne leczenie noworodka koncentratami czynników krzepnięcia. Podejrzenie krwawienia do głowy wymaga szybkiej diagnozy i niezwłocznego rozpoczęcia leczenia. Jeśli nie wdroży się na czas odpowiedniego leczenia wówczas takie krwawienia staje się stanem zagrażającym życiu dziecka i może być przyczyną trwałego uszkodzenia mózgu. Najistotniejsze w akcji porodowej jest indywidualne podejście lekarzy do Ciebie jako pacjentki oraz Twoje zaufanie do personelu przyjmującego poród. Pamiętaj, że ten artykuł ma jedynie funkcję informacyjną i nie zastępuje konsultacji lekarskich. Wszelkie szczegółowe informacje przekaże Ci Twój lekarz hematolog oraz ginekolog prowadzący Twoją ciążę. Na podstawie:1. Górska-Kosicka M, Odnoczko E, Windyga J. Ciąża, poród i połóg u nosicielki hemofilii. Hematology in Clinical Practice, Vol 7, No 1 (2016)#447162. https://hemophilianewstoday.com/pregnancy-and-hemophilia/3. https://www.cdc.gov/ncbddd/hemophilia/women.html4. https://www.haemophilia.org.au/about-bleeding-disorders/women-with-bleeding-disorders/carrying-the-haemophilia-gene/pregnancy5. Carriers and women with hemophilia, World Federation of Hemophilia

27 grudnia 2022
Czy pojawienie się krwiomoczu może zaniepokoić chorego lub opiekuna osoby chorej na hemofilię? Nasza ekspertka, dr Irena Woźnica-Karczmarz, wyjaśnia wątpliwości i odpowiada na pytanie, które zadała mama chłopca chorego na hemofilię na czacie naszego portalu. Pojawienie się krwi w moczu powinno zaniepokoić każdego, a chorych na hemofilię skłonić do pilnego kontaktu z Ośrodkiem Leczenia Hemofilii w celu uzyskania porady. Jeśli krew zabarwia mocz, mówi się o widocznym albo makroskopowym krwiomoczu. Jeśli krew jest wykrywana tylko w badaniach laboratoryjnych, wówczas mówi się o mikroskopowym krwiomoczu. Krwiomocz jest częstym problemem występującym w ogólnej populacji, dotyczy około 16% młodych dorosłych mężczyzn i około 21% mężczyzn po 50. roku życia. Jest to także dość częsta przypadłość u chorych z hemofilią. Na podstawie przeprowadzonych badań szacuje się, że do 66% chorych na hemofilię doświadcza krwiomoczu w ciągu swojego życia. W trakcie krwiomoczu mocz może mieć kolor czerwony lub brązowy, zależnie od ilości krwi i pory dnia. Uważa się, że już 1 ml krwi w moczu może spowodować zmianę zabarwienia. W godzinach porannych mocz może przybierać barwę ciemnobrązową ze względu na zagęszczenie po nocy, w ciągu dnia może być różowy lub czerwony. Do krwawienia może dojść w każdej części układu moczowego, począwszy od nerek, poprzez moczowody, pęcherz moczowy, a skończywszy na gruczole krokowym. Przyczyn krwiomoczu może być bardzo wiele. Najczęstszą przyczyną są infekcje, inne przyczyny to obecność małych kamyczków lub piasku w drogach moczowych, bardzo intensywne ćwiczenia fizyczne, aktywność seksualna, niektóre leki czy też urazy okolicy narządów płciowych. Krwiomocz jest także częstym objawem występującym u starszych mężczyzn z przerośniętą prostatą. Bardzo rzadko przyczyną krwiomoczu mogą być nowotwory pęcherza, nerek lub prostaty. Pomimo, że u chorych z hemofilią zaleca się leczenie każdego krwawienia, w przypadku wystąpienia krwiomoczu postępowanie jest odmienne. Nie wolno stosować ani czynników krzepnięcia, ani kwasu traneksamowego (Exacylu) w tabletkach. Zawsze, w razie pojawienia się wątpliwości, należy skontaktować się z lekarzem Ośrodka Leczenia Hemofilii. Jest to bardzo ważne, ponieważ nigdy nie wiadomo w jakiej części dróg moczowych doszło do krwawienia, a standardowe leczenie czynnikiem krzepnięcia czy kwasem traneksamowym może spowodować powstanie dużego skrzepu, mogącego zablokować nerkę lub moczowód, powodując ogromne dolegliwości bólowe i uszkodzenie nerki. Może także dojść do powstania dużego skrzepu w pęcherzu moczowym i zatrzymania moczu. W przypadku krwiomoczu u chorych z hemofilią zaleca się odpoczynek i ograniczenie aktywności fizycznej. Należy zwiększyć ilość spożywanych płynów do 2-3 litrów dziennie, unikać kwaśnych soków, takich jak pomarańczowy, grejpfrutowy czy pomidorowy, a także napojów wysokosłodzonych, np. lemoniady czy coca-coli. Nie wolno pić także alkoholu i kawy. Jeśli nie doszło do urazu, nie ma dolegliwości bólowych o charakterze palenia, pieczenia itp., wraz z moczem nie wypływają skrzepy krwi, a mocz nie ma nieprzyjemnego zapachu, to z reguły wystarczy odpoczynek i nawodnienie. Krwiomocz ustąpi samoistnie po 2-3 dniach. Wizyta u lekarza jest konieczna zawsze, kiedy w moczu pojawią się skrzepy krwi, występuje ból pleców, ból w boku lub ból brzucha, jeśli krwiomocz nasila się w czasie, jeśli mocz ma nieprzyjemny zapach i jest mętny, gdy w trakcie oddawania moczu pojawia się piekąco-palący ból, jeśli pojawi się gorączka lub złe samopoczucie albo jeśli krwawienie jest związane z urazem w okolicy nerki. W przypadku krwiomoczu lekarz zleci wykonanie analizy moczu. Jeśli w moczu są obecne bakterie, konieczne jest zastosowanie antybiotyku. Jeśli krwiomocz trwa dość długo, konieczne będzie wykonanie badania morfologii krwi, aby ocenić jej stan. W przypadku bólu konieczne będzie wykonanie badania USG, tomografii komputerowej lub cystoskopii, aby ocenić stan nerek, dróg moczowych i pęcherza moczowego. Jeśli krwiomocz powtarza się, wówczas konieczna jest wizyta u urologa. U mężczyzn po 40. roku życia wskazana jest wizyta u urologa już po pierwszym epizodzie krwiomoczu. W bardzo rzadkich przypadkach, kiedy krwiomocz nie ustępuje, a brak jest konkretnej przyczyny krwawienia, lekarz może zalecić podanie w warunkach szpitalnych małych dawek czynnika krzepnięcia wraz z forsowanym nawadnianiem dożylnym, aby przepłukać nerki. Należy zapamiętać, że: Krwiomocz dość często pojawia się u chorych z hemofilią. W trakcie krwiomoczu nie wolno stosować czynników krzepnięcia ani kwasu traneksamowego. Sam krwiomocz, bez towarzyszącego bólu, gorączki, nieprzyjemnego zapachu moczu nie wymaga leczenia, ale konieczny jest 2-3 dniowy odpoczynek i odpowiednie nawadnianie. Pojawienie się bólu, gorączki, mętnego moczu, skrzepów krwi w moczu, złego samopoczucia wymaga pilnego kontaktu z lekarzem. Krwiomocz pojawiający się u mężczyzn powyżej 40. roku życia wymaga konsultacji urologicznej. Krwiomocz utrzymujący się u chorego z hemofilią dłużej niż kilka dni wymaga zgłoszenia się do szpitala i przeprowadzenia badań diagnostycznych. Wracając do odpowiedzi na pytanie mamy chłopca chorego na hemofilię: Nie każdy chory na hemofilię doświadczy krwiomoczu. Szansa na pojawienie się krwiomoczu może dotyczyć około 66% chorych na hemofilię, przy czym u części chorych krwiomocz może pojawić się jednorazowo, a u niektórych chorych może nawracać. Przyczyny krwiomoczu są tu takie same, jak u osób bez hemofilii. Krwiomocz nie jest efektem przyjmowania czynnika krzepnięcia. Regularne, profilaktyczne stosowanie czynnika krzepnięcia jest obecnie złotym standardem leczenia hemofilii i zmniejsza ryzyko wystąpienia krwawień, także krwawień z dróg moczowych oraz uszkodzenia nerek spowodowanego odkładaniem się żelaza uwolnionego z hemoglobiny. Powtarzające się epizody krwiomoczu wynikają z osłabienia funkcji nerek i występowania chorób przewlekłych nerek, które wymagają pilnej diagnostyki i leczenia. Zmienione na różowo lub czerwono zabarwienie moczu nie zawsze jest rzeczywistym krwiomoczem. Należy pamiętać, że niektóre pokarmy mogą powodować zmianę zabarwienia moczu. Po spożyciu buraczków, botwinki, jeżyn i jagód mocz może przybierać barwę od różowej aż do czerwonej, a po spożyciu rabarbaru może być brązowy. W przypadku spożycia dużej ilości czerwonych buraków zmiana zabarwienia moczu może utrzymywać się nawet przez kilka dni. Jeżeli masz jakiekolwiek pytanie dotyczące choroby jaką jest hemofilia, zachęcamy do zadania pytania naszemu Ekspertowi.

22 grudnia 2022
Wszystkiego Dobrego z Okazji Świąt Bożego Narodzenia i nadchodzącego Nowego Roku 2023, dużo miłości, wiary, spokoju serca, pokoju w naszych społecznościach, radości i szczerego uśmiechu, który dodaje otuchy oraz nadziei rozjaśniającej ciemności, życzy Redakcja portalu Hemopozytywni.pl

20 grudnia 2022
Niania jest jedną z pierwszych osób, którym powierzasz swoje dziecko. Obawy związane z pozostawieniem dziecka z kimś innym niż członek rodziny są zrozumiałe. Wybór właściwej opiekunki do dziecka to ważna decyzja. Tym istotniejsza, gdy Twoje dziecko ma zdiagnozowaną hemofilię lub inne zaburzenie krwawienia. Nie należy jednak na wyrost budować atmosfery strachu i zagrożenia. Dziecko z hemofilią to przede wszystkim… dziecko. Nie zapominajmy o tym. Jak znaleźć osobę, która właściwie zaopiekuje się naszym dzieckiem? Poniżej opisujemy pewne narzędzia, które mogą pomóc w podjęciu dobrej decyzji. I. Jak powiedzieć innym o zaburzeniu krwawienia u dziecka? Upewnij się, że Twoja wiedza o zaburzeniach krwawienia u dziecka jest aktualna i pochodzi ze sprawdzonych źródeł. Ważne jest również, jaki rodzaj hemofilii i jak ciężkiej posiada dziecko. Dobrze byłoby, gdybyś posiadał/a broszury informacyjne dot. skaz krwotocznych, które mogłabyś/mógłbyś przekazać. Bądź przygotowany/a do odpowiadania na pytania. O broszury możesz poprosić lekarza albo znaleźć je na stronach Polskiego Stowarzyszenia Chorych na Hemofilię (http://www.hemofilia.org.pl) lub portali edukacyjnych hemostaza.edu.pl oraz hemopozytywni.pl Skonsultuj się z lekarzem lub innym rodzicem dziecka z hemofilią, aby uzyskać sugestie dotyczące zagadnień, o których warto wspomnieć. Przemyśl wszystkie możliwe reakcje rozmówcy i sposób, w jaki możesz na nie zareagować. Omów znaczenie ochrony prywatności w kontekście informacji o zaburzeniach krwawienia u Twojego dziecka. Zarezerwuj wystarczająco dużo czasu na rozmowę, aby mówić dokładnie, bez przyspieszania i omijania informacji. Kiedy przekażesz wszystkie informacje, ustalcie z potencjalną opiekunką czas na odpowiedź i podjęcie decyzji przez obie strony. II. Kluczem jest komunikacja Często jako rodzic potrzebujesz kilku krótkich zdań, aby wyjaśnić innym zaburzenia krwawienia dziecka. To przykładowa informacja dla niani, którą możesz dostosować do swoich potrzeb: Mój syn/córka [IMIĘ DZIECKA] ma zaburzenie krwawienia zwane [NAZWA ZABURZENIA]. Oznacza to, że w jego/jej krwi brakuje białka, które pomaga jej prawidłowo krzepnąć. Moje dziecko nie wykrwawi się na śmierć, a w przypadku skaleczenia lub zadrapania nie będzie krwawić szybciej niż inni. Jeśli wymagana jest pierwsza pomoc, przebiega tak samo jak u zdrowego dziecka. Chcę być jednak powiadomiona/y, jeśli uderzy się w głowę, poskarży się na silny ból lub upadnie z dużej wysokości. Proszę o kontakt, jeśli będzie miało poważniejsze obrażenia, ponieważ będę musiał/a podać mu leki. Zachęcamy nasze dziecko do udziału w niektórych sportach i zajęciach ruchowych, takich jak [PODAJ PRZYKŁADY], ale nie w sportach kontaktowych, takich jak piłka nożna czy zapasy. Chętnie odpowiem na wszelkie pytania. Tak, jak ważne jest znalezienie odpowiedniego opiekuna dla Twojego dziecka, tak istotne jest utrzymanie z nim dobrej komunikacji i klimatu otwartości. Oto kilka wskazówek: ● Pytaj opiekunki: Co moje dziecko zrobiło dzisiaj? Jak się czuje moje dziecko? Czy są jakieś problemy, o których powinienem/powinnam wiedzieć?● Wyrażaj swoje obawy dotyczące Twojego dziecka, np.: Moje dziecko jest wyjątkowo ciche; Moje dziecko wydaje się unikać poruszania jedną z kończyn. Nigdy nie bój się zadawać pytań. Zadawanie pytań pomoże Ci lepiej zrozumieć potrzeby Twojego dziecka oraz potrzeby, pytania i obawy opiekuna. III. Kto pyta, nie błądzi Aby współpraca miała mocne podstawy, obie strony mają prawo, a nawet obowiązek pytać o różne aspekty opieki nad dzieckiem. Pytania do potencjalnych opiekunek Czy pracowała Pani kiedyś jako opiekunka do dziecka? W jakim wieku były dzieci i jak długo Pani się nimi zajmowała? Czy kiedykolwiek opiekowała się Pani dzieckiem z problemami zdrowotnymi? Dlaczego chce Pani pracować z dziećmi? Jakie grupy wiekowe lubi Pani najbardziej/najmniej? Dlaczego? W jakiej grupie wiekowej czuje się Pani najlepiej? Czy woli Pani pracować z chłopcami czy dziewczynkami? Dlaczego? Czy kiedykolwiek była Pani w sytuacji nagłej podczas opieki nad dzieckiem? Jak Pani sobie z nią poradziła? W jakiej sytuacji zadzwoniłaby Pani do mnie? W jakim momencie zadzwoniłaby Pani pod numer alarmowy? Czy mieszka Pani w pobliżu? Czy może Pani zapewnić sobie transport? (dużym ułatwieniem dla obu stron jest sytuacja, w której niania mieszka blisko rodziny, u której pracuje). Czy ma Pani jakieś ograniczenia zdrowotne, które mogłyby wpłynąć na Pani zdolność do opieki nad dzieckiem? Czy w pobliżu znajduje się Pani znajomy lub członek rodziny, z którym może się Pani skontaktować w razie nagłego wypadku? Czy kiedykolwiek podawała Pani leki dziecku, którym się opiekowała? Czy wie Pani co zrobić, gdy dziecko się zakrztusi? Jakie zajęcia zazwyczaj wykonuje Pani z dziećmi w wieku mojego dziecka? Czy ma Pani referencje od innych rodziców? Opcjonalnie: Czy brała Pani udział w kursach szkoleniowych z zakresu opieki nad dziećmi? Czy ma Pani certyfikat z zakresu pierwszej pomocy? Pytania, które opiekunka może zadać rodzicom: Niania także może martwić się trudnościami związanymi z opieką nad dziećmi ze specjalnymi potrzebami zdrowotnymi. Niektóre wątpliwości mogą dotyczyć pierwszej pomocy przy drobnych skaleczeniach, zadrapaniach czy uderzeniach, a przede wszystkim – obawy przed wzięciem na siebie zbyt dużej odpowiedzialności. Co muszę wiedzieć o stanie zdrowia Państwa dziecka? Czy dziecko ma jakieś alergie pokarmowe, wymaga specjalnych leków lub ma inne specjalne potrzeby? Na jakie objawy u dziecka świadczące o krwawieniu powinnam zwrócić uwagę? Co należy zrobić, jeśli wystąpi krwawienie? Jak mogę się z Państwem kontaktować (numery telefonów komórkowych, telefony do zakładu pracy)? Czy mogą Państwo podać nazwiska, numery i adresy kilku pobliskich przyjaciół, sąsiadów lub krewnych, z którymi mogłabym się skontaktować w szczególnym przypadku? W jakich okolicznościach powinnam się z Państwem skontaktować? Kiedy należy zadzwonić pod numer alarmowy, a kiedy do Państwa? Czy są jakieś czynności, których Państwa dziecko nie może wykonywać lub zabawy, w których nie powinno uczestniczyć ze względu na zaburzenia krzepnięcia? Jakie zabawy są odpowiednie? Jeśli muszę podawać leki, czy mogą Państwo dostarczyć pisemne instrukcje i pokazać mi, co będę musiała zrobić? Możesz zaproponować opiekunce skontaktowanie jej z inną nianią dziecka z hemofilią, która pomoże rozwiać wątpliwości i podzieli się z nią swoim dotychczasowym doświadczeniem (o kontakt możesz spytać innego rodzica dziecka z hemofilią, który korzysta z usług opiekunki). IV. Zestaw materiałów informacyjnych dla opiekunki Po znalezieniu odpowiedniej opiekunki, warto zostawić jej komplet podstawowych materiałów informacyjnych. Upewnij się, że opiekunka wie, gdzie je znaleźć oraz że są łatwo dostępne i umieszczone razem z lekami, które mogą się przydać. Kiedy zostawiasz swoje dziecko z opiekunką lub opiekunem, zawsze: Upewnij się, że numery telefonu służbowego i komórkowego są wyraźnie zapisane. Zapisz numery alarmowe i adres domu dużą czcionką i umieść w widocznym miejscu (to ważna informacja w przypadku konieczności wezwania pogotowia ratunkowego). Rozważ przeprowadzenie testowego skontaktowania się z Tobą w nagłym wypadku. Upewnij się, że opiekun rozróżnia rodzaje sytuacji, które wymagają i nie wymagają kontaktu z Tobą. V. Zostałaś właśnie opiekunką dziecka ze skazą krwotoczną? Opieka nad dzieckiem z zaburzeniami krwawienia może Cię martwić. Przede wszystkim musisz jednak wiedzieć, że dziecko z zaburzeniami krwawienia jest jak każde inne dziecko. Lubi robić te same rzeczy, które uwielbiają inne dzieci. Poza byciem nieco czujniejszą w kwestii nadzoru i posiadaniem obowiązkowej znajomości podstawowych procedur nagłych, możesz cieszyć się opieką nad dzieckiem tak samo jak w innych przypadkach. Kluczowa jest tu rozmowa i dobra komunikacja z rodzicem dziecka z zaburzeniami krzepnięcia. Im więcej wiesz o samym zaburzeniu i konkretnym dziecku, tym pewniej i bardziej komfortowo będziesz się czuła, spędzając z nim czas. Źródło: https://stepsforliving.hemophilia.org/first-step/child-care-and-school/babysitters-and-play-dates

14 grudnia 2022
Ulubione utwory kojarzące się z ważnymi momentami naszego życia, rytmy pobudzające do tańca czy melancholijne brzmienia wprowadzające w zamyślenie. Zgodzimy się chyba wszyscy, że muzyka towarzyszy nam bardzo często. Dlaczego by więc nie wykorzystać jej wpływu w dbaniu o swoje zdrowie? – Muzyka łączy ludzi z otaczającą ich rzeczywistością, kulturą, środowiskiem. Ale jednocześnie dotyka tego co „wewnątrz” nas (...) może odprężać lub dawać energię, zmieniać nastawienie i emocje, stymulować rozwój poznawczy, pobudzać wyobraźnię, dawać siłę do walki i wspierać duchowo – stwierdza dr hab. Krzysztof Stachyra z Uniwersytetu Marii Curie-Skłodowskiej w Lublinie, pedagog muzyczny i certyfikowany muzykoterapeuta. Słuchanie muzyki angażuje kilka regionów mózgu, w tym te, które wpływają na emocje, poznanie, odczuwanie i ruch. Całkiem więc prawdopodobne, że może również pomóc w leczeniu problemów w tych obszarach. Muzyka? Mam to we krwi Polskie Stowarzyszenie Muzykoterapeutów definiuje muzykoterapię jako proces, w którym wykwalifikowany muzykoterapeuta posługuje się muzyką w celu przywracania zdrowia, poprawy funkcjonowania lub wspierania rozwoju osób z różnymi potrzebami emocjonalnymi, fizycznymi, umysłowymi. Praca z odpowiednio wykształconym muzykoterapeutą może przynieść wiele korzyści, ocenić potrzeby pacjenta, jego gust i zainteresowania. Muzykoterapią w ścisłym tego słowa znaczeniu nie jest samodzielne słuchanie muzyki, ale i ono może nieść ze sobą pozytywne skutki, a przede wszystkim – przyjemność! Zachęcamy do słuchania muzyki zawsze wtedy, kiedy przychodzi na to ochota i gdy są ku temu właściwe warunki. Co ciekawe, pozytywny wpływ na organizm ma nie tylko słuchanie muzyki, ale i czynne jej tworzenie i wykonywanie. Może to czas, aby odkryć w sobie pasję do grania na instrumencie, założenia zespołu czy komponowania piosenek? Dawno, dawno temu… Pomysł, że muzyka może mieć moc terapeutyczną nie jest wcale taka „młoda” (choć może się taką wydawać). Platon i Arystoteles pisali, że muzyka wpływa na ludzkie dusze i ma wartość edukacyjną. Muzykoterapia jako formalna praktyka rozwinęła się w następstwie I i II wojny światowej. Lekarze zajmujący się hospitalizowanymi weteranami zauważyli, że stan ich pacjentów poprawił się zarówno pod względem fizycznym, jak i emocjonalnym po tym, jak lokalni muzycy odwiedzali szpital i grali w nim koncerty. Takie działanie miało łagodzić fizyczne i emocjonalne traumy wyniesione z frontu. Muzyka kontra ból Prawdopodobnie słyszeli Państwo o haju biegacza, kiedy to podczas wymagającej sesji ćwiczeń fizycznych, jego mózg uwalnia endorfiny – substancje chemiczne przynoszące poczucie euforii, radości i spełnienia. Muzyka pobudza mózg do produkcji tych samych endorfin. Muzyka, czy to słuchana przez nas, czy wykonywana, może pomóc łagodzić ból związany z wieloma dolegliwościami i przynosi korzyści ludziom w każdym wieku. Muzykoterapia jest metodą, którą eksperci nazywają „wsparciem proceduralnym", czyli pomocą dla pacjenta w przechodzeniu przez bolesną lub wywołującą strach procedurę leczenia. Wiele ścieżek, wykorzystywanych przez mózg do przetwarzania muzyki to te same ścieżki, które przetwarzają ból. Jeśli więc mózg jest skupiony, na przykład, na koncercie Mozarta, nie pozostaje mu wiele miejsca na przekazywanie informacji o bólu pochodzącym z ciała. Muzyka może również pomóc zrelaksować się i zmniejszyć odczuwany niepokój. Oprócz zmniejszania jednorazowego bólu, muzyka może również wpływać na przewlekły ból, spowodowany różnymi schorzeniami. Jak słuchać? Trzy kroki do muzycznej podróży 1. Wybór playlisty Warto zacząć od wyboru muzyki, która sprawia, że czują się Państwo dobrze. Wybierajmy to, co lubimy, bez względu na gatunek - nie wstydźmy się swoich wyborów, ale próbujmy też szukać nowej muzyki - odkryjemy niejedną muzyczną perełkę. 2. Poczujmy rytm Polecamy słuchać, nucić lub śpiewać zawsze, gdy tego Państwo potrzebują. Badania medyczne udowadniają, że muzyka może wpływać na nasze tętno, uspokajać bądź pobudzać. 3. Uwaga na głośność Zbyt głośne odtwarzanie muzyki, zwłaszcza jeśli nosimy słuchawki douszne, może uszkodzić słuch. Zachęcamy do pamiętania o tym i odpowiedzialnego słuchania. Na podstawie: https://hemaware.org/mind-body/healing-power-music https://teologiapolityczna.pl/antonina-karpowicz-zbinkowska-antyczna-koncepcja-muzyki-jako-speculum-musicae https://www.umcs.pl/pl/komentarze-eksperckie,22097,muzykoterapia-komentarz-ekspercki,113129.chtm

24 listopada 2022
Z przyjemnością ogłaszamy, że w prestiżowym konkursie projektowania graficznego, nominację otrzymały dwie realizacje graficzki Anety Lewandowskiej, które powstały z naszej inicjatywy. Są to: projekt bloga naszego „Hemopozytywni.pl", oraz zeszyt kreatywny „Staś i Hemofilia", książka aktywizująca małego czytelnika, przybliżająca temat hemofilii. Jak czytamy na stronie wydarzenia, Projekt Roku 21/22 „analizuje najbardziej przełomowe realizacje twórców grafiki użytkowej w Polsce oraz promuje wartości bliskie Stowarzyszeniu Twórców Grafiki Użytkowej". Nominacja cieszy tym bardziej, że wspólnie zrealizowane z Anetą Lewandowską projekty przybliżają zagadnienia hemofilii u dzieci i młodzieży. Głos małych pacjentów wybrzmiewa więc głośno dzięki świetnej graficznej oprawie. Z dumą prezentujemy obie realizacje i gratulujemy projektantce kolejnego sukcesu: Hemopozytywni Serwis internetowy ma charakter edukacyjny i pomaga w budowaniu świadomości na temat hemofilii. Głównym celem projektu jest pomoc zarówno dla młodzieży, jak i dzieci, w znalezieniu sposobu na wyrażanie siebie pomimo choroby. Strona ma zachęcić do działania, podkreślając ważność profilaktyki. Umożliwia stworzenie więzi i znajomości z innymi chłopcami (na hemofilię chorują tylko mężczyźni).Tworzy wspierającą społeczność oraz zaufane miejsce.Treści publikowane na blogu mają na celu udzielania faktycznego wsparcia w codzienności życia z chorobą. Strona jest uzupełniana sukcesywnie, treści są wciąż aktualizowane. Staś i hemofilia – zeszyt kreatywny Poza warstwą merytoryczną publikacja zawiera polecenia zachęcające małego czytelnika do działań plastycznych, takich jak rysowanie, klejenie, wycinanie, itd. Dzięki działaniom podejmowanym przez dziecko książka staje się kompletną historią, a każdy z egzemplarzy jest jedyny w swoim rodzaju. Publikacja jest darmową broszurą, dzięki czemu ma szansę dotrzeć do szerokiego grona odbiorców. Realizacja obu projektów była możliwa dzięki zaufaniu i wsparciu firmy Takeda. Warto również wspomnieć, że to kolejne bardzo istotne wyróżnienie tego typu projektów. W 2020 roku nagrodę główną prestiżowej Polish Graphic Design Awards zdobyła zaprojektowana przez Anetę Lewandowską, a wydana przez nas książeczka „Igor i jego tajemnicze przygody – czyli historia chłopca z ITP". Więcej informacji o projektach znajdą Państwo na stronie konkursu Projekt Roku

10 listopada 2022
.... czyli jak oswoić siebie i dziecko ze zmianą w nowym środowisku? O nowych wyzwaniach jakie czekają zarówno na dziecko, jak i rodzica w szkole czy w przedszkolu opowie dr Marta Rusek – psycholog. https://vimeo.com/757690782

8 listopada 2022
… czyli jak zapewnić bezpieczeństwo dziecku z hemofilią w nowym środowisku? O „patentach” i sprawdzonych rozwiązaniach w tej kwestii opowie rodzic dziecka z hemofilią, Ewa Cichacka. https://vimeo.com/757690706

31 października 2022
... czyli ćwiczenia fizyczne, sport, aktywność zalecane czy niewskazane? O aktywności fizycznej dostosowanej do potrzeb oraz możliwości dziecka z hemofilią opowie lek. med Anna Badowska. https://vimeo.com/757690849

25 października 2022
... czyli jak przygotować dziecko, siebie i otoczenie do nowego etapu w życiu. O profilaktyce krwawień mówi dr n. med. Elżbieta Latos-Grażyńska. https://vimeo.com/757690812

4 października 2022
Mamy wspaniałą wiadomość dla wszystkich czytelników portalu hemopozytywni.pl! Od 1 października aktywna jest nowa zakładka: PYTANIE DO EKSPERTA. Przy pomocy tego modułu każdy użytkownik może zadać pytanie dotyczące hemofilii naszemu ekspertowi. Wyczerpująca odpowiedź lekarza hematologa zostanie opublikowana na naszej stronie w ciągu dwóch tygodni. Jeżeli masz jakiekolwiek wątpliwości dotyczące hemofilii, zachęcamy Cię do skorzystania z tego narzędzia. PYTANIE DO EKSPERTA

13 lipca 2022
Zapraszamy na spotkanie online dla rodziców dzieci z hemofilią dotyczące przygotowań do nowego etapu życia dziecka, czyli pójścia do przedszkola i szkoły. Specjaliści odpowiedzą na pytania uczestników, rozwieją wątpliwości oraz przekażą pewną wiedzę na temat, który może budzić niepewność i strach u rodziców. Webinar odbędzie się 13 września o godz. 18:00. Program wydarzenia: 18.00-18.30Czym jest kompleksowa opieka nad dzieckiem chorym na hemofilię. Profilaktyka krwawień, czy personalizacja ma znaczeniedr n. med Elżbieta Latos-Grażyńska18.30-19.00Ćwiczenia fizyczne, sport, aktywność zalecane czy niewskazane?lek. med Anna Badowska 19.00-19.30Podzielmy się doświadczeniem: Jak zapewnić bezpieczeństwo dziecku z hemofilią w nowym środowisku. „Patenty” i sprawdzone rozwiązaniaEwa Cichacka - rodzic dziecka z hemofilią 19.30-20.15Nowe środowisko: Przedszkole i szkoła – jak oswoić siebie i dziecko ze zmianądr Marta Rusek - psycholog 20.15-20.30Dyskusja Link do spotkania

4 lipca 2022
Wakacje ruszyły pełną parą i każdy z nas planuje większe lub mniejsze podróże. Przedstawiamy kilka wskazówek dotyczących podróżowania z hemofilią bez zbędnych trosk i zmartwień. Zadbaj o ubezpieczenie na podróż W zależności od tego dokąd zmierzasz, ważne jest, aby zadbać o ubezpieczenie podróżne, które w swoich warunkach obejmuje istniejące choroby przewlekłe. Niektórzy z nas posiadają ubezpieczenie, które może obejmować również podróż. Jednak warto upewnić się, czy obejmuje ono również istniejące choroby przewlekłe, takie jak hemofilia A. Dlatego sprawdź warunki swojego ubezpieczenia, gdyż podróż do szpitala oraz leczenie w obcym kraju bez ubezpieczenia może być bardzo kosztowne. Zaopatrz się w wystarczającą ilość czynnika Upewnij się, że przygotowałeś na podróż wystarczającą ilość czynnika. Bez względu na rodzaj czynnika, który stosujesz, ważne, abyś miał ze sobą taką ilość czynnika, jakiej potrzebujesz gdy jesteś poza domem (i zapas na wypadek nagłych sytuacji). Oznacza to również zapakowanie wystarczającej ilości igieł, bandaży i środków odkażających. Wszyscy wiemy, że bagaż czasami się gubi, więc dobrze jest mieć je ze sobą również w bagażu podręcznym. Większość linii lotniczych nie pobiera dodatkowej opłaty za bagaż podręczny. Spakuj leki Upewnij się, że wszystkie leki na receptę, których potrzebujesz, masz zapakowane w oryginalne opakowania do torby podręcznej. Pamiętaj, aby wziąć ze sobą wystarczającą ilość leków, która wystarczą na cały czas podróży. Leki i paszport są najważniejszymi rzeczami potrzebnymi podczas podróży, wszystkie inne zawsze można kupić na miejscu. Nie zapomnij swojej karty informacyjnej Podczas podróży dobrze jest zabrać ze sobą kartę informacyjną od lekarza. Karta może zawierać informacje na temat koncentratu czynnika, który przyjmujesz oraz wszelkich potrzebnych leków na receptę, a także Twojego planu leczenia na wypadek konieczności udania się do szpitala. Rozpoznaj okolicę Dobrą zasadą jest sprawdzenie, czy miejsce, do którego się wybierasz, ma w okolicy centrum leczenia hemofilii. Jeśli tak, możesz skontaktować się z kliniką i poinformować ich, że planujesz podróż do ich miasta (lub pobliskiego miasta). Listę ośrodków leczenia hemofilii można znaleźć w Internecie. Poszukuj Społeczność chorych na hemofilię jest bardzo zżyta i pomocna. W dużych miastach istnieją zazwyczaj grupy wsparcia dla chorych na hemofilię, do których można dotrzeć i zasięgnąć od nich informacji podczas podróży. Mogą pomóc Ci poruszać się w nowym otoczeniu, a nawet wskazać jakieś lokalne atrakcje do odwiedzenia! Nie bój się prosić o pomoc Niezależnie od tego, czy podróżujesz sam czy z ukochaną osobą, nigdy nie bój się prosić o pomoc. Podróżowanie z ciężkim bagażem może być kłopotliwe. Większość linii lotniczych oferuje wózki inwalidzkie oraz pomoc przy bramce, z której warto skorzystać. Jeżeli zadzwonisz do linii lotniczej z wyprzedzeniem, możesz poprosić o dodatkową przestrzeń na nogi lub o specjalne miejsce siedzące. Noś bransoletkę medyczną Każdy pacjent z przewlekłą chorobą powinien przez cały czas nosić bransoletkę medyczną lub naszyjnik (jest to przydatna wskazówka, nawet gdy nie podróżujesz). Na rynku jest wiele stylowych ofert takich produktów, których zakup warto rozważyć przed podróżą. Śledź swoje podania czynnika Upewnij się, że prowadzisz rzetelny rejestr swoich podań podczas podróży. W ten sposób na bieżąco możesz śledzić, ile czynnika wziąłeś. Po powrocie do domu możesz omówić wszelkie wątpliwości z hematologiem. Najważniejsze: baw się dobrze! Jeśli jesteś odpowiednio przygotowany, podróżowanie będzie niezwykle ekscytującą zabawą (nawet z chorobą krwi). Staraj się nie dopuścić, aby stres związany z nieznanym powstrzymał Cię od cieszenia się podróżą i eksplorowania świata. Źródło: healthline.com

30 maja 2022
Zapraszamy do obejrzenia relacji ze spotkania online dla rodziców małych dzieci z hemofilią, które odbyło się 11 kwietnia o godz. 18:00. Podczas webinaru specjaliści: dr Danuta Pietrys - hematolog oraz dr Marta Rusek - psycholog opowiedziały jak opiekować się dzieckiem z nowo rozpoznaną hemofilią pod kontem medycznym a także jak sobie psychicznie radzić z wyzwaniami jakie stawia przed rodzicem hemofilia szczególnie u świeżo upieczonych rodziców. Na spotkaniu nie zabrakło również doświadczonej mamy Malgorzaty Kubery, która starała się wesprzeć psychicznie wszystkich rodziców oraz podzieliła się swoimi sposobami na oswojenie siebie i malucha z chorabą. https://www.youtube.com/watch?v=F8DvKyJVHfY&t=4648s

Hemofilia jest wrodzoną skazą krwotoczną spowodowaną obecnością nieprawidłowego genu, który odpowiada za produkcję czynnika krzepnięcia VIII lub IX. Pomimo, że hemofilia jest chorobą krwi, to jednak objawy jej towarzyszące najczęściej dotyczą narządu ruchu, mowa tu o wylewach do stawów. Przedstawiamy Państwu broszurę edukacyjną autorstwa dr Ireny Woźnicy, z której możemy się dowiedzieć jak rozpoznać krwawienie u dziecka z hemofilią, co zrobić gdy takie wystąpi oraz jak im zapobiegać VV-MEDMAT-64086, 04/2024

Narodziny dziecka z hemofilią całkowicie zmieniają życie rodziny. Pojawia się wiele problemów i pytań, na które trudno jest znaleźć właściwe odpowiedzi. Przewodnik ten, skierowany jest do opiekunów i rodziców chorych dzieci, opisuje hemofilię, przybliża problemy dnia codziennego, odpowiada na podstawowe pytania dotyczące objawów występujących w hemofilii i możliwości leczenia, ale przede wszystkim radzi, jak postępować, aby ochronić dziecko przed zagrożeniami. W całej Polsce zostały powołane regionalne i lokalne ośrodki leczenia hemofilii i właśnie tam każdy rodzic chorego dziecka powinien się udać, aby uzyskać profesjonalną pomoc. Informacje o wszystkich ośrodkach leczenia hemofilii można znaleźć na stronie internetowej Narodowego Centrum Krwi. Kiedy w rodzinie przychodzi na świat dziecko z hemofilią, bardzo istotne jest wsparcie, które można uzyskać od innych chorych i ich rodzin. Zachęcamy do zapoznania się z Przewodnikiem dla rodziców, autorstwa dr Ireny Woźnicy, w którym znajdują się odpowiedzi na wiele pytań dotyczących hemofilii.

25 maja 2022
Diagnoza hemofilii - i co dalej? Hemofilia jest chorobą dziedziczną. Mutacje spontaniczne, które pojawiają się w rodzinie po raz pierwszy, występują w 30-40% przypadków. Choroba jest dużym zaskoczeniem i wiąże się ze sporym strachem i wątpliwościami - mało kto się jej spodziewa, toteż rodzice muszą się mierzyć z pewnymi wyzwaniami w opiece nad dzieckiem z tą chorobą. Jak leczymy dziecko chore na hemofilię? na żądanie (w przypadku krwawienia, urazu, nagłego zdarzenia). Takie leczenie jest stosowane u małych dzieci do 1. roku życia.profilaktyczne – podawanie koncentratu czynnika krzepnięcia, zapobiegawczo, kilka razy w tygodniu. Optymalną profilaktyką jest profilaktyka spersonalizowana, dostosowana do masy ciała chorego, lokalizacji krwawień, trybu życia, fenotypu i specyficznej dla danego chorego charakterystyki działania czynnika w organizmie danego pacjenta. W Polsce wszyscy chorzy mają dostęp do leczenia domowego – mogą korzystać z czynnika w domu i tam go przechowywać. Dziećmi z hemofilią i innymi skazami krwotocznymi w Polsce zajmują się ośrodki znajdujące się przy oddziałach onkologii i hematologii dziecięcej. W kraju znajduje się 17 takich instytucji. Pracuje w nich zespół specjalistów złożony z lekarzy różnych specjalizacji i pielęgniarek. Dziecko z hemofilią w Polsce objęte jest także programami terapeutycznymi: Narodowym Programem Leczenia Chorych na Hemofilię i Pokrewne Skazy KrwotoczneProgramem Zapobiegania Krwawieniom u Dzieci z Hemofilią A i B Po pierwsze – profilaktyka W opiece nad dzieckiem z hemofilią najważniejsza jest profilaktyka krwawień. Istotne jest unikanie urazów, używanie kasków czy ochraniaczy podczas uprawiania sportów, zakaz uprawiania sportów kontaktowych (np. boks, judo, karate). Nie zwalniamy dziecka z zajęć wychowania fizycznego, lecz pilnujemy, aby aktywność fizyczna była przystosowana do ich możliwości. Zakazane jest wykonywanie zastrzyków domięśniowych. Istotne jest także unikanie niesteroidowych leków przeciwzapalnych typu Nurofen, Ibufen - osłabiają one krzepnięcie krwi. Profilaktyka w hemofilii pozwala poprawić jakość życia chorego, ochronić jego stawy, umożliwia dziecku uprawianie wymarzonego sportu, pozwala na realizowanie marzeń i chodzenie do szkoły czy przedszkola – jest więc bardzo istotna, a jej pomijanie prowadzi do ciężkich powikłań stawowych, ograniczających bądź uniemożliwiających normalne, bezbolesne poruszanie się i funkcjonowanie. Objawy hemofilii u noworodka Noworodek z hemofilią jest narażony na krwawienia w różnych częściach ciała, m.in. do mięśnia uda, z kikuta pępowiny czy wewnątrz czaszki. Standardami postępowania u noworodka płci męskiej nosicielki genu hemofilii (kiedy hemofilia występuje w rodzinie) jest oznaczenie aktywności czynnika krzepnięcia z krwi pępowinowej. Wykonuje się USG głowy i jamy brzusznej oraz bacznie się go obserwuje, a szczepienia wykonuje się u niego od początku drogą podskórną. Czasami przy typowym opiekowaniu się małym dzieckiem, podnoszeniu czy obejmowaniu może dojść do wystąpienia sińców (pod pachami, na klatce piersiowej). U 6-miesięcznego i starszego dziecka, kiedy zaczyna raczkować i więcej się poruszać, stawiać pierwsze kroki, zdarzają się pierwsze krwawienia pourazowe, z dziąseł czy języka, domięśniowe a także siniaki np. na kolanach. Jak zaobserwować krwawienia u małego dziecka? Jak rozpoznać krwawienia do stawu (łokciowego, kolanowego, skokowego)? Obserwujemy, że dziecko utyka, nie opiera pięty na podłożu czy nie prostuje w pełni kolana, jego ruchomość jest ograniczona, okolica danego stawu jest nadmiernie ocieplona, pojawia się obrzęk i bolesność, a dziecko przy próbie poruszenia kończyną płacze. Krwawienia w niektórych lokalizacjach mogą zagrażać życiu. Są to krwawienia do ośrodkowego układu nerwowego (OUN), ściany gardła, z przewodu pokarmowego, do jamy brzusznej. Jak postępować w przypadku krwawienia? Układamy kończynę tak, aby nie była obciążona. Dziecko często samo kładzie ją w położeniu, w którym boli ona najmniej.Stosujemy zimne okłady (krótko).Unieruchamiamy kończynę (krótko).Podajemy leki przeciwbólowe.Podajemy czynnik (w odpowiedniej ilości).Obserwujemy reakcję na podany czynnik.Po wylewie do mięśnia czy stawu bardzo ważna jest fizjoterapia - aby staw czy mięsień mógł powrócić do stanu sprawności sprzed krwawienia bądź zbliżonego.W przypadku krwawień zagrażających życiu - podajemy czynnik i wzywamy karetkę pogotowia. A co ze szczepieniami i infekcjami u dzieci z hemofilią? Szczepienia W żadnym przypadku nie zwalniamy dzieci z hemofilią ze szczepień. Szczepienia wymagane u dzieci przez polski system ochrony zdrowia są podawane hemofilikom zawsze w formie podskórnej. Zaleca się stosowanie szczepionek wieloskładnikowych, dzięki temu ilość wkłuć jest mniejsza. Infekcje W przypadku infekcji o łagodnym przebiegu, które nie wymagają stosowania antybiotyków, udajemy się po poradę do pediatry. Lekiem przeciwgorączkowym najbezpieczniejszym dla hemofilików jest Paracetamol. Bezwzględnie należy unikać inwazyjnych zabiegów, np. stawiania baniek. W przypadku kataru i kaszlu warto stosować łagodne preparaty, takie jak woda morska oraz leki zmniejszające nasilenie kaszlu. Zaleca się stosowanie leków uszczelniających naczynia krwionośne i poprawiających odporność (niespecyficznych immunostymulatorów). Co jest szczególnie ważne w opiece nad dzieckiem z hemofilią? Baczna obserwacjaOcena stanu stawów przed snemProfilaktyczne podawanie czynnika ranoWażne jest regularne podawanie czynnika krzepnięcia, dostosowane do rytmu dnia dziecka (np. nauki szkolnej)Profilaktyczne podawanie czynnika przed większym wysiłkiem fizycznymBardzo ważne jest prowadzenie dzienniczka, który umożliwia monitorowanie leczenia małego pacjenta

23 maja 2022
Psycholożka i psychoterapeutka dzieci i młodzieży dr Marta Rusek na webinarze „Jak opiekować się dzieckiem z nowo rozpoznaną hemofilią w 1. roku życia: Rady doświadczonych Ekspertów" przedstawiła cenne rady z zakresu psychologicznych aspektów opieki nad noworodkiem z tym schorzeniem. Każde dziecko potrzebuje przede wszystkim stałej, stabilnej opieki i miłości.Przyjmij i zaakceptuj, że czasem w opiece nad dzieckiem będziesz potrzebować wsparcia z zewnątrz. Nie bój się przyjmować i prosić o to wsparcie.Pojawiające się trudne emocje są naturalne i prowadzą do nowej rzeczywistości (o ile nie trwają długo i nie mają niezmiennie silnego natężenia). Akceptacja choroby to proces.Szukaj wiedzy na temat choroby i angażuj się w działanie, np. stowarzyszeń dla rodziców dzieci z hemofilią – to daje nadzieję i poczucie sprawczości.Warto, aby ojciec dziecka był równie silnie zaangażowany w opiekę nad dzieckiem i jego leczenie.Dziecko potrzebuje spokojnych, obecnych rodziców, przestrzeni do rozwoju fizycznego, stałego rytmu dobowego i stałego miejsca zamieszkania.Jako rodzic dziecka nie zapominaj o swoich potrzebach - wiedzy, snu i odpoczynku, rozmowy, poczucia bezpieczeństwa i wsparcia itp.Pamiętaj o potrzebach zdrowego rodzeństwa. W rozmowie z dziećmi przedstawiaj chorobę jako wyzwanie, z którym mierzycie się wszyscy razem.Potrzeby emocjonalne niemowlaka nigdy nie są manipulacją i powinny być zawsze zaspokajane.Buduj więź z dzieckiem poprzez dotyk, uśmiech, słowa, obecność i odpowiadanie na jego potrzeby. Pamiętaj, że więź z dzieckiem buduje się już od pierwszych chwil ciąży.Bolesne zabiegi medyczne w pierwszych chwilach życia nie powinny być wykonywane przez mamę – dotyk mamy ma koić i uspokajać, a na wykonywanie zabiegów przez rodziców przyjdzie czas później.Pierwszy rok życia dziecka jest bazą dla jego poczucia wartości, ważności, poczucia siebie i swojego ciała.

17 maja 2022
Pani Małgorzata Kubera, mama 9-letniego Gucia z ciężką postacią hemofilii A podzieliła się swoimi doświadczeniami ze słuchaczami webinaru. O chorobie Gucia rodzina wie od 8 lat – w pierwszym roku rozwoju synka nie wiedziano o hemofilii. W rodzinie Gucia hemofilia nie występowała, dlatego nikt się jej nie spodziewał. Na początku rodzicom towarzyszył szok, co jest naturalne przy tego typu informacjach. Jak odkryto hemofilię? Częste siniaczenie u chłopca zwróciło uwagę bliskich, a pediatra skierował chłopca na dalszą diagnostykę w kierunku skazy krwotocznej. Od razu zastosowano profilaktykę, zastrzyki podawano w szpitalu. Prelegentka wspomina te wizyty jako traumę. W pewnym momencie, jak mówi, przychodzi jednak moment, kiedy dziecko samo podaje rączkę i przyzwyczaja się do procedury podawania czynnika krzepnięcia. Momenty zwątpienia pojawiają się i później, nawet po przyzwyczajeniu się dziecka do zastrzyków, ale i one mijają. Początki są najtrudniejsze, ale wszystkiego można się nauczyć. To, co mogą zrobić rodzice małego „hemoludka”, jak wspomina pani Małgorzata, to przygotowanie siebie samego oraz mieszkania do opieki nad dzieckiem. Dostosowanie mieszkania Oklejony stół, komoda, główne krawędzie mebli – obecnie na rynku mnóstwo jest różnego koloru pianek i gąbek, które można użyć w tym celu. Najważniejsze – rodzice mają się z tym dobrze czuć. Jeśli uważają, że to będzie dla ich dzieci najlepsze rozwiązanie, warto tak zaaranżować mieszkanie, nie zważając na głosy innych czy wstyd, który może się budzić w rodzicu – „Jak to, będziemy mieć tak oklejone mieszkanie? A co kiedy przyjdą znajomi, rodzina?” Na pierwsze lata dzieciństwa Gucia dało to spokój i psychiczny komfort. warto jednak szanować siebie nawzajem oraz czyjeś wybory – można to zrobić, ale nie trzeba; nie oceniajmy wyborów innych rodziców dzieci z hemofilią. Przy małych, aktywnych dzieciach w wieku 2-4 lat jest to trudne zadanie, ale musimy obserwować „ścieżki”, którymi lubi biegać dziecko. Pilnujmy, aby zamykać drzwi. Dobrym patentem w przypadku Gucia okazał się sam materac na podłodze zamiast łóżka. Gucio przez kilka lat, do 6 roku życia nocował właśnie na materacu, unikając obijania się o wyższy i twardy mebel. Dywany i maty pod dywan, które amortyzują dziecko podczas uczenia się chodzenia czy raczkowania są także dobrym rozwiązaniem. Aktywność fizyczna Aktywność fizyczną należy dostosowywać do możliwości swojego dziecka, np. wyjście na rower czy hulajnogę wybierajmy w dniu podawania czynnika. Kask – jest to poważna decyzja, nie jest on bowiem wygodny. Niektórzy rodzice są jego zwolennikami, inni przeciwnikami. Wybór należy do opiekuna dziecka. Warto stosować ochraniacze na poszczególne części ciała, np. nakolanniki czy ochraniacze na nadgarstki. Podawanie czynnika w domu Mama Gucia zachęciła do podawania dzieciom czynnika w domu. Dzięki temu rodzina odzyskuje pewną wolność i samodzielność. Często z tyłu głowy, np. podczas wyjazdów pojawia się pytanie, gdzie na wszelki wypadek znajduje się najbliższy ośrodek leczenia hemofilii czy szpital. Mimo to, profilaktyka dzięki podawaniu czynnika w warunkach domowych jest o wiele wygodniejsza. Pani Małgorzata poleca krem Emla, który miejscowo znieczula miejsce wkłucia igły. Jest także zwolenniczką zmieniania żył wybieranych do zastrzyków, np. co pół roku – aby uczyć się zwalczać bariery psychiczne i mieć więcej pewnych miejsc dostępnych do wkłucia. Rozmowy z dzieckiem Od najmłodszych lat warto rozmawiać z dzieckiem, tłumacząc o co chodzi w chorobie, na miarę jego zdolności poznawczych i językowych. Można tłumaczyć dziecku na czym polega hemofilia, dlaczego czasem boli go kolano lub nie robią mu się strupki. Ważne, aby dziecko było świadome dlaczego otrzymuje zastrzyki. Kiedy pyta – odpowiadajmy zgodnie z prawdą, nie „zbywając” czy spłycając zagadnienie. Pani Małgorzata przytoczyła swój sposób tłumaczenia choroby Guciowi – „Ja noszę okulary. Mam zepsuty wzrok, muszę nosić taki aparacik, aby coś widzieć. Ty masz hemofilię i otrzymujesz zastrzyki. Dziadka bolą kolana, więc nosi kule.” Co z przedszkolem i szkołą? Gucio chodził do zwykłego, państwowego przedszkola, które przyjęło go bardzo dobrze (był tam pierwszym dzieckiem z hemofilią). Czego rodzice mogą wymagać od przedszkola, do którego chodzi syn? Jeśli coś się zdarzy, personel powinien niezwłocznie powiadomić o tym rodziców, podając godzinę zdarzenia, ponieważ to zapewne któryś z rodziców przyjedzie, aby podać czynnik dziecku. Guciowi zdarzyły się dwa niegroźne i typowe dla dzieci przedszkolnych „wypadki” (upadek, uderzenie główką), ale wszystko się dobrze skończyło. Pani Małgorzata trzymała także na wszelki wypadek dawkę czynnika krzepnięcia wraz ze sprzętem do podawania w przedszkolu – dyrekcja oraz Sanepid wyraziły na to zgodę. Mama Gucia ma zaufaną pielęgniarkę – to osoba, na której pomoc można liczyć w sytuacjach wyjątkowych. Oswajanie ze sprzętem do podawania czynnika Zastrzyk czyli ziuk – tak nazywa je pani Małgorzata wraz z synkiem. Warto od najmłodszych lat zaznajamiać dzieci ze sprzętem do wykonywania zastrzyków, oczywiście przy zachowaniu zasad sterylności. Niech dzieciak bierze w tym udział, aby były mu one coraz bardziej znane. Gucio miał okres fascynacji zastrzykami, które wykonywał na… swoich przytulankach. Atrakcyjną metodą na wzbudzenie ciekawości u dziecka jest używanie kolorowych plasterków – przyklejenie takiego plastra, które wybierze dziecko to mała „nagroda” po zastrzyku.

10 maja 2022
11 kwietnia br. brałam udział w webinarze organizowanym przez portal Hemopozytywni.pl o tytule „Jak opiekować się dzieckiem z nowo rozpoznaną hemofilią w 1. roku życia: Rady doświadczonych Ekspertów". Całe spotkanie było bogatym źródłem informacji i pomogło mi uporządkować to, co wiem na temat hemofilii oraz rozwiać niektóre moje wątpliwości, jako rodzica opiekującego się dzieckiem z tą skazą krwotoczną. Strach przed nieznaną chorobą ustąpił wiedzy, podanej w przyjazny sposób. Ekspertkami webinaru były: Dr Danuta Pietrys, która wygłosiła wykład z perspektywy lekarskiej;Pani Małgorzata Kubera, mama Gucia, która była głosem rodziców mierzących się z wyzwaniem hemofilii u dziecka;Dr Marta Rusek, psycholożka. Spotkanie poprowadziła pani Ewa Cichacka, mama Mikołaja, chłopca z hemofilią. Głos zabrał także Bogdan Gajewski, Prezes Polskiego Stowarzyszenia Chorych na Hemofilię. Na początku spotkania krótko przedstawiono nowy, atrakcyjny portal Hemopozytywni.pl, skierowany do dzieci, młodzieży i rodziców pacjentów z hemofilią. Powstał on, aby tworzyć społeczność, pomagać, edukować nas rodziców i bawić nasze dzieci. Pani dr Danuta Pietrys we wstępie wykładu w skrócie opisała poszczególne postacie hemofilii (ciężką, umiarkowaną i łagodną), ich objawy (którymi są głównie krwawienia do stawów, mięśni i tkanek miękkich), powikłania i leczenie. Pani Doktor następnie omówiła dokładnie objawy, jakie możemy zaobserwować u małych dzieci z hemofilią w przypadku wystąpienia krwawień do stawów czy mięśni. Im szybciej zaobserwuje się nieprawidłowości, tym wcześniej można zareagować i zapobiec poważniejszym powikłaniom zdrowotnym. Później ekspertka przedstawiła techniczne uwarunkowania i sposoby podawania czynnika krzepnięcia w domu. W ośrodkach leczenia hemofilii czy na warsztatach edukacyjnych rodzice, krewni lub już same dzieci (gdy są odpowiednio starsze) mogą nauczyć się sprawnie podawać koncentrat czynnika krzepnięcia. Dowiedziałam się, że w opiece nad dzieckiem z hemofilią najważniejsza jest profilaktyka krwawień. Nie należy także bać się szczepień wymaganych u małych dzieci oraz aktywności fizycznej dostosowanej do ich możliwości. Pani Małgorzata Kubera dodawała otuchy rodzicom małych „hemoludków”, z uśmiechem, spokojem, a miejscami nawet z żartem opowiadając o swoim doświadczeniu, nawet o tych trudnych momentach. Stwierdziła, że każdy rodzic wytwarza poniekąd swoją metodę na życie z hemofilią. Opowiedziała o swoich sposobach na wychowywanie hemofilika od najmłodszych lat. Podkreśliła, jak istotna jest wolność w podejmowaniu decyzji dotyczących wychowania dziecka z hemofilią. Zachęciła do uczestnictwa w spotkaniach rodziców i dzieci z hemofilią – to podnosi na duchu i wspomaga, utwierdza w wybranej drodze i umożliwia nawiązanie nowych kontaktów i przyjaźni. Z pewnością z tej zachęty skorzystam. Punkt widzenia mamy dziecka z hemofilią z pewnością jest bardzo potrzebny nam, którzy dopiero zaczynamy mierzyć się z tą chorobą. Spokój w głosie pani Małgorzaty uspokoił mnie. Jak się okazuje – strach ma wielkie oczy. I mówię to nie po to, aby umniejszać istotę choroby jaką jest hemofilia, bo to oczywiście poważna sprawa, ale po to, aby powiedzieć tym, którzy to czytają i sobie samej – że naprawdę można zaopiekować się dzieckiem z hemofilią i będzie ono szczęśliwie rosnąć i się rozwijać, tak jak inne dzieci w jego wieku. Ostatnim wykładem było wystąpienie Pani dr Marty Rusek, psycholożki, która zaprezentowała psychologiczne aspekty opieki nad dzieckiem z hemofilią w 1. roku życia. 1. rok życia to okres, w którym dzieci rozwijają się w ogromnym tempie i budują sobie bazę pod różne umiejętności; także wtedy rodzi się silna więź z mamą i tatą. Dużą część wykładu stanowiły informacje o rodzicach, ponieważ to od ich opieki uzależnione są dzieci w okresie noworodkowym. Dowiedzieliśmy się, że opiekun dziecka nie istnieje w próżni i to bardzo ważne, aby od początku wiedział, skąd może czerpać pomoc i wsparcie (oprócz swojego partnera). Małe dzieci nie mają świadomości swojej choroby, natomiast informacja o hemofilii może wpłynąć silnie na jego rodziców, dziadków – na otoczenie. W uczuciach często to mama czuje, jakby chorowała razem z dzieckiem. Akceptacja informacji o chorobie wiedzie przez różne emocje, jakimi mogą być strach, złość, izolacja, żal – ich akceptacja wiedzie do konstruktywnego działania. Ważne jest, aby rodzice chorego dziecka nie zapominali także o swoich potrzebach. Często zapomina się także o zdrowym rodzeństwie dziecka z hemofilią – a każdy członek rodziny nie powinien poczuć się osamotniony. To ważne, aby wprowadzać dzieci w zagadnienie choroby, lecz nie strasząc, a opisując ją jako wyzwanie. Na końcu specjaliści odpowiedzieli na pytania uczestników webinaru. Webinar był owocnym spotkaniem, w którym jak w “pigułce” zawarto kluczowe i potrzebne informacje na temat opieki nad małym dzieckiem z hemofilią. Z pewnością przyczynił się do poszerzenia wiedzy na ten temat i rozwiał niektóre wątpliwości związane z chorobą. Bardzo dziękuję za tego typu inicjatywy i czekam na następne webinary o tematyce opieki nad dziećmi z hemofilią – w różnym wieku.

7 kwietnia 2022
Zapraszamy na spotkanie online dla rodziców małych dzieci z hemofilią. Specjaliści odpowiedzą na pytania uczestników, rozwieją wątpliwości oraz przekażą pewną wiedzę na temat, który może budzić niepewność i strach, szczególnie u świeżo upieczonych rodziców. Webinar odbędzie się 11 kwietnia o godz. 18:00. Program wydarzenia: 18.00-18.10Idea spotkań oraz prezentacja bloga dla Dzieci i Rodziców hemopozytywni.plEwa Cichacka – Mama Mikołaja18.10-18.40Opieka nad dzieckiem chorym na hemofilię w 1. roku życiaDr Danuta Pietrys – lekarz hematolog18.40-19.00Opieka nad dzieckiem okiem doświadczonych RodzicówMałgorzata Kubera – Mama Gucia19.00-19.45Psychologiczne aspekty opieki nad dzieckiem z hemofilią w 1. roku życiaDr Marta Rusek – psycholog 19.45-20.30Dyskusja Link do spotkania

9 lutego 2022
15 grudnia 2021 roku odbyło się spotkanie podsumowujące sierpniowy HemoCamp, czyli obóz dla chłopaków ze skazą krwotoczną. Super było chociaż internetowo zobaczyć znajome twarze i porozmawiać, zwyczajnie pogadać o naszym życiu - tym “zwyczajnym”, o szkole, planach na ferie, kolegach i marzeniach. Hemocamp wszystkim chłopakom dał dużo dobrego i zmotywował ich do walki z trudnościami życia z hemofilią. Te trudności nie są tak straszne, gdy można profesjonalnie i pewnie podać samemu sobie czynnik krzepnięcia. Obóz był na pewno inspirującym zdarzeniem. Jeden z nas nawet na spotkaniu wspomniał, że dzięki niemu myśli o zawodzie pielęgniarza w przyszłości. Na początku Hubert opowiedział wszystkim o naszym portalu Hemopozytywni.pl, która została stworzona dla młodzieży i dzieci z hemofilią. Potem głos zabrał Piotrek, który opowiedział o swoich doświadczeniach z HemoCampu - oczywiście pozytywnych. Jak mówił, obóz dał jego uczestnikom bardzo wiele, przede wszystkim umiejętność podawania sobie czynnika. Dzięki temu nie jesteśmy “uzależnieni” od swoich rodziców, opiekunów czy szpitala. “Po raz pierwszy miałem tak naprawdę okazję, aby podzielić się z kimś innym, również chorującym na hemofilię, moimi problemami codziennymi oraz tym jak sobie z tym życiem radzę. Relacje między nami hemofilikami się wzmocniły.” - powiedział Piotr. Następnie głos zabrali opiekunowie HemoCampu. Zapewnili, że w czasie po obozie również pozostają dla nas wsparciem. Prof. Paweł Łaguna z radością rozmawiał z nami i pytał, co u nas słychać. Nie krył dumy z tego, że po powrocie do domu chłopaki naprawdę korzystają z nabytej umiejętności samodzielnego podawania czynnika. Pani psycholog Karina Tomczyk na Campie prowadziła bardzo ciekawe gry i zabawy oraz opowiadała o znaczeniu pozytywnego podejścia do życia. Teraz również przywitała nas z entuzjazmem i porozmawiała chwilę o naszych planach oraz odczuciach z obozu. Obejrzeliśmy profesjonalny, krótki film, streszczający w sobie wakacyjny wyjazd. Jeszcze raz mogliśmy wrócić do letnich wspomnień świetnej zabawy. Na końcu każdy mógł zabrać głos, a nawet pokazać się, jeśli miał kamerkę i nie wstydził się zbyt mocno. Znalazło się kilku odważnych. Super zobaczyć kolegów po kilku miesiącach bez kontaktu. Potem każdy chętny mógł wypełnić ankietę dotyczącą spotkania, tego co się w nim podobało, a co mniej oraz wyrazić chęć dalszego spotykania się w takim gronie oraz współpracy z portalem Hemopozytywni.pl. Czym był Hemocamp? Był tygodniowym wyjazdem dla chłopaków ze skazą krwotoczną, na którym mogli nauczyć się, jak zyskać samodzielność dzięki podawaniu sobie czynnika, bez udziału personelu medycznego, rodziców czy innych dorosłych. Poza tym, był fajnym wakacyjnym sposobem spędzenia czasu z rówieśnikami - poprzez ćwiczenia, basen, ognisko, gry integracyjne. Tam chłopaki mogli porozmawiać o swoich problemach z kolegami, którzy przeżywają podobne trudności. Mam nadzieję, że projekt obozu dla młodych hemofilików będzie kontynuowany w przyszłości, i że jeszcze nieraz spotkamy się - na żywo bądź w internecie. Świetnie jest wiedzieć, że nie jest się samemu ze swoimi przeżyciami, trudnościami i marzeniami! https://www.youtube.com/watch?v=ZxoYoDcfwWo
22 września 2021
Hemofilia to genetyczna choroba krwi zaliczana do grupy osoczowych skaz krwotocznych. Istotą choroby jest wrodzony brak lub niedobór czynników krzepnięcia krwi. U zdrowej osoby – jeśli naczynie krwionośne (żyła, tętnica, naczynie włosowate) zostanie uszkodzone, elementy krwi, płytki (trombocyty) oraz czynniki krzepnięcia, tworzą skrzep i zapobiegają przedłużonemu krwawieniu. U osób z hemofilią – ze względu na brak lub niedobór czynników krzepnięcia tworzenie się skrzepu jest utrudnione, dlatego dochodzi do wydłużenia czasu krwawienia (zewnętrznego, np. z nosa, lub wewnętrznego, np. do stawów)1 Typy hemofilii: A Najczęściej spotykana odmiana choroby. Cierpiący na nią nie mają wystarczającej ilości czynnika krzepnięcia krwi VIII. B Rzadziej występujący. W tym przypadku istnieje niedobór czynnika IX. Hemofilia typu A i B głównie dotyczy mężczyzn. C Tu występuje niedobór XI czynnika krzepnięcia krwi. Ten typ hemofilii dotyczy głównie Żydów aszkenazyjskich. Typ C dotyczy zarówno kobiet jak i mężczyzn.

Uniwersytecki Dziecięcy Szpital Kliniczny im. Ludwika ZamenhofaKlinika Onkologii i Hematologii Dziecięcej UM w Białymstoku15-274 Białystok, ul. Waszyngtona 17tel. 85 74 50 846 - Sekretariat Kliniki Onkologii i Hematologii Szpital PediatrycznyI Oddział Wewnętrzny43-300 Bielsko-Biała, ul. Sobieskiego 83tel. 33 812 5000 do 4 w. 250 Szpital Uniwersytecki im. dr A. JuraszaKlinika Pediatrii, Hematologii i Onkologii85-094 Bydgoszcz, ul Skłodowskiej-Curie 9tel. 52 585 48 60 - sekretariat Chorzowskie Centrum Pediatrii Odział Hematologii i Onkologii Dziecięcej41-500 Chorzów, ul. Truchana 7tel. 32 3490043, 32 3490075, 32 3490000 Wojewódzki Szpital Specjalistyczny im. Najświętszej Maryi Panny Oddział Dziecięcy42-200 Częstochowa, ul. Bialska 104/118tel. 34 367 36 18 (pielęgniarki); 34 367 36 12, 34 367 36 20 (sekretariat) Samodzielny Publiczny Szpital Kliniczny nr 1 GUM w GdańskuKlinika Chorób Dzieci80-211 Gdańsk, ul. Dębinki 7tel. 58 349 28 63, 58 349 28 70 / 58 349 28 80 (klinika chorób dzieci) Szpital nr 1 Oddział Pediatrii44-100 Gliwice, ul. Kościuszki 29tel. 32 461 32 77 (oddział pediatrii), 32 461 32 77 (sekretariat oddziału pediatrii) w. 287, 277 Górnośląskie Centrum Zdrowia Dziecka i MatkiOddział Onkologii, Hematologii i Chemioterapii40-752 Katowice, ul. Medyków 16tel. 32 207 18 00, 32 207 17 63 (oddział onkologii, hematologii i chemioterapii) Wojewódzki Szpital Zespolony Świętokrzyskie Centrum Pediatrii im. Władysława BuszkowskiegoII Klinika Pediatrii – Oddział Onkologii i Hematologii Dziecięcej25-736 Kielce, ul. Grunwaldzka 45, Pawilon Gtel. 41 361 55 25 (centrala), 41 347 05 60 (gabinet lekarski) Samodzielny Publiczny Dziecięcy Szpital Kliniczny CM UJKlinika Onkologii i Hematologii Dziecięcej30-522 Kraków Prokocim, ul. Wielicka 265tel. 12 658 20 11 Uniwersytecki Szpital DziecięcyKlinika Hematologii i Onkologii20-093 Lublin, ul. Chodźki 2tel. 81 743 00 10 (centrala), 81 718 55 20 (oddział hematologii i onkologii) Centralny Szpital Kliniczny, Ośrodek Pediatryczny im. M. KonopnickiejPoradnia Hematologiczna97-738 Łódź, ul. Sporna 36/50tel. 42 617 77 77 (centrala szpitala); 42 617 77 57 (pok. lek. oddział VI); 42 617 77 32 (oddział VII) Wojewódzki Specjalistyczny Szpital DziecięcyOddział Wewnętrzny 1, Hematologiczno-Onkologiczny10-561 Olsztyn, ul. Żołnierska 18atel. 89 533 77 01 (centrala), 89 539 33 71 (oddział hematologii) Wojewódzkie Centrum MedyczneOddział Pediatrii45-418 Opole, ul. Witosa 26tel. 77 45 20 798 Oddział Chorób Wewnętrznych i HematologiiSpecjalistyczny ZOZ nad Matką i Dzieckiem61-825 Poznań, ul. B. Krysiewicza 7/8tel. 61 850 62 78 / 61 850 62 79 (dyrekcja) Kliniczny Szpital Wojewódzki nr 2 im. Św. Jadwigi Królowej w RzeszowieKlinika Onkohematologii Dziecięcej35-301 Rzeszów, ul. Lwowska 60sekretariat tel.: 17 86 64 588, gab. lek.: 17 86 64 558, pielęgniarki: 17 86 64 601 Samodzielny Publiczny Szpital Kliniczny nr 1 PUM Klinika Chorób Dzieci Oddział Hematologii i Onkologii Dziecięcej71-252 Szczecin, ul. Unii Lubelskiej 1tel. 91 425 31 39; 425 35 39 / 91 425 30 00 (centrala) Katedra i Klinika Pediatrii, Hematologii i Onkologii WUM; SPDSK02-091 Warszawa, ul. Żwirki i Wigury 63APokój lekarski - 22 317 96 17 lub 22 317 96 14, poradnia 22 317 91-89 / 88, pokój pielęgniarek hematologia - 22 317 96 51, oddział dzienny - hematologia 22 317 96 23, centrala szpitala - 22 317 91 64, lekarz dyżurny - 790 338 596e-mail: hematologia@spdsk.edu.pl Klinika Onkologii i Hematologii Dziecięcej AM50-345 Wrocław, ul. Bujwida 44tel. 71 328 20 40 Samodzielny Miejski Publiczny Szpital Kliniczny nr 1 im. prof. Stanisława Szyszko UMŚKlinika Hematologii Dziecięcej41-800 Zabrze, ul. 3 Maja 13/15tel. 32 370 43 72, fax 32 273 60 75 Wojewódzki Szpital Kliniczny im. Karola Marcinkiewicza Sp. z o. o.ul. Zyty 26, 65-045 Zielona GóraKliniczny Oddział Onkologii i Hematologii Dziecięcejtel.: 534 694 931, 534 460 221 (całodobowy) Kliniczny Oddział Pediatrii z Pododdziałami: Endokrynologii, Diabetologii i Nefrologii Dziecięcejtel.: 603 566 271, 68 32 96 392 (całodobowy) e-mail: sekretariat@szpital.zgora.plszpital.zgora.pl

21 września 2021
Przedstawiamy Wam niezwykły przewodnik. Jest to krótka broszura informacyjna dla pacjentów z hemofilią i ich rodzin jest broszurą autorstwa dr Ireny Woźnicy-Karczmarz. W tej niewielkiej książeczce znajdziecie przydatne informacje dotyczące choroby, jej diagnostyki oraz leczenia, a także dotyczące żywienia czy rozwoju emocjonalnego dziecka obciążonego skazą krwotoczną. Pobierz przewodnik w wersji PDF

10 czerwca 2021
Sport sprawia ogromną przyjemność, za sprawą endorfin, które wytwarzają się w naszym ciele. To takie związki które powodują, że jesteśmy zadowoleni. Dlatego bardzo ważne byśmy starali się być bardzo aktywni. Czasami strach przed urazem sprawia, że boimy się aktywności, ale to właśnie systematyczne ćwiczenia pozwalają na prowadzenie aktywnego i bezpiecznego a przede wszytskim radosnego stylu życia. Obejrzyj film i zobacz jak w bezpieczny sposób ćwiczyć i mieć frajdę z treningu. https://www.youtube.com/watch?v=C_UqpXEkkc4&list=PLIl5xXIitHCOMXvCRYaupQWpE7GMN0zgo https://www.youtube.com/watch?v=WbzlSSN1jWI&t=8s

Jak wygląda codzienność chłopca z hemofilią? Czy można być aktywnym fizycznie chorując na skazę krwotoczną? Ksawery jest najlepszym przykładem, że sport i hemofilią mogą chodzić w parze. Przedstawiamy Wam Ksawerego - super piłkarza, który oprócz piłki nożnej uwielbia jeździć na crosie po sadzie swoich rodziców. Zobaczcie sami jak wygląda życie naszego bohatera, o którym niezwykle opowiada w krótkim materiale filmowym. https://vimeo.com/603843787